下列表格中的各种情况,可以用下图的曲线表示的是( )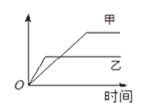
| |
反 应 |
纵坐标 |
甲 |
乙 |
| A |
相同质量的氨,在同一容器中 2NH3 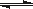 N2 + 3H2 ΔH<0 N2 + 3H2 ΔH<0 |
氨气的转化率 |
500℃ |
400℃ |
| B |
等质量钾、钠分别与足量水反应 |
H2质量 |
钠 |
钾 |
| C |
在体积可变的恒压容器中,体积比1︰3的N2、H2,N2 + 3H2 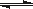 2NH3 2NH3 |
氨气的浓度 |
活性高的催化剂 |
活性一般的催化剂 |
| D |
2 molSO2和1 molO2,在相同温度下2SO2 + O2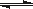 2SO3 2SO3 |
SO3物质的量 |
2个大气压 |
10个大气压 |
下列说法中正确的是()
①只有一种元素组成的物质,一定是纯净物;②所有酸性氧化物都是非金属氧化物;③硝酸和氢硫酸均既有氧化性又有还原性;④化学反应的实质就是旧化学键断裂、新化学键形成的过程。
| A.①② | B.③④ | C.①②④ | D.都正确 |
右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是()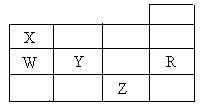
| A.常压下五种元素的单质中,Z单质的沸点最高 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.W的氢化物的沸点比X的氢化物的沸点高 |
| D.Y元素的非金属性比W元素的非金属性强 |
下列关于丙烯(CH3—CH =CH2)的说法正确的()
| A.丙烯分子有8个σ键,1个π键 |
| B.丙烯分子中3个碳原子都是sp3杂化 |
| C.丙烯分子存在非极性键 |
| D.丙烯分子中3个碳原子在同一直线上 |
下列说法中错误的是:()
A.SO2、SO3都是极性分子 |
B.在NH4+和[Cu(NH3)4]2+中都存在配位键 |
C.元素电负性越大的原子,吸引电子的能力越强 |
D.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性 |
据报道,有科学家用激光将置于铁室中石墨靶上的碳原子炸松,与此同时再用射频电火花喷射氮气,此时碳、氮原子结合成碳氮化合物薄膜。据称,这种化合物可能比金刚石更坚硬。其原因可能是( )
| A.碳、氮原子构成平面结构的晶体 |
| B.碳氮键比金刚石中的碳碳键更短 |
| C.氮原子最外层电子数比碳原子最外层电子数多 |
| D.碳、氮的单质化学性质均不活泼 |