(1)在一个容积为3L的密闭容器内进行如下反应:N2(气)+3H2(气)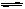 2NH3
2NH3
(气)。反应开始时,n(N2)=1.5mol,n(H2)= 4.4mol,2min后达到平衡状态,n(H2)=3.5mol。
用NH3的浓度变化来表示该反应的反应速率为___________________,2min末N2的浓度
________________,平衡时N2的转化率为______________________。
(2)在密闭容器中,对于反应:N2(g)+ 3H2(g)  2NH3(g),在反应起始时N2和H2分别
2NH3(g),在反应起始时N2和H2分别
为5mol和15mol,当达到平衡时,N2的转化率为20%。若以NH3为起始反应物,反应条
件与上述反应相同时,欲使其达到平衡时各成分的百分含量与前者相同,则NH3的起始物
质的量为 ,NH3的转化率 。
A、B、C、D是短周期元素形成的四种气体单质。E、F均为气体,且F为红棕色。有关的转化关系如下图所示(反应条件均已略去)。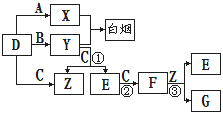
请回答下列问题:
(1)D的化学式为、Y的化学式为、E的化学式为. (2)反应③的离子方程式为。
(3)Y和E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为
(4)0.1 mol·L-1的X溶液和0.1 mol·L-1的Y溶液等体积混合,溶液呈___性(填“酸”、“碱”或“中”),原因是_____________(用离子方程式说明)。
现有四瓶丢失标签的NaOH、Na2CO3、AlCl3、NH4HSO4溶液,为鉴别四瓶溶液,将四瓶溶液编号为A、B、C、D进行实验。实验过程和记录如下图所示(无关物质已经略去):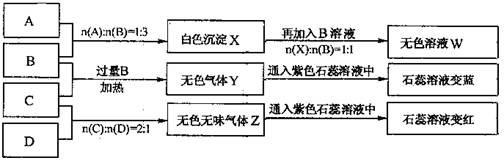
请回答:
(1)A、W的溶液分别加热蒸干并灼烧最后所得固体为、(填化学式)。
(2)D溶液pH(填“<”、“>”或“=”)7,原因是(用离子方程式表示)。
(3)等物质的量浓度的A、B、C、D溶液pH由大到小的顺序是NaOH> .> >
NH4HSO4。(用化学式表示)
(4)等物质的浓度的C溶液与NH4Cl溶液相比较,c(NH4):前者后者(填“<”、“>”或“=”)。
(5)若在稀溶液中B、C按物质的量之比2:1反应,则离子方程式为
(7分)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题: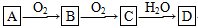
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体.
①D的化学式是________;
②在工业生产中B气体的大量排放被雨水吸收后形成了________而污染了环境.
(2)若A在常温下为气体,C是红棕色的气体.
①A、C的化学式分别是:A________;C________.
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式___________________________.该反应________(填“属于”或“不属于”)氧化还原反应.
平衡指的是两个相反方向的变化最后所处的运动状态;在平衡时,两种变化仍在继续进行,但是它们的速率相等;根据变化的性质可分为物理平衡和化学平衡,中学阶段涉及的平衡有气体可逆反应的平衡、酸碱电离平衡、水解平衡及沉淀-溶解平衡等等。
(1)现有容积为1 L的恒温恒容密闭容器,向其中加入2 mol A气体和2 mol B气体后发生如下反应:
A(g) + B(g)  C(g)△H= - a kJ·mol-1
C(g)△H= - a kJ·mol-1
20s后,反应达到平衡状态,生成1 mol C气体,放出热量Q1kJ。回答下列问题。
①计算20s内B气体的平均化学反应速率为___________,写出该反应的平衡常数表达式___________。
②保持容器温度和容积不变,若改为向其中加入1molC气体,反应达到平衡时,吸收热量Q2kJ,则Q1 与Q2的相互关系正确的是____________(填字母)。
(A)Q1 + Q2 = a(B) Q1 + 2Q2 < 2a(C)Q1 + 2Q2 > 2a(D)Q1 + Q2 < a
③在原平衡基础上,保持容器温度和容积不变,向容器中再通入b mol A气体(b>0)时,v(正)_____v(逆)(填“>”、“<”或“=”),重新达平衡后,C气体的平衡体积分数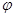 (C) =
(C) = 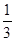 ,则b = ____________。
,则b = ____________。
(2)常温下,将VmL、0.1000mol·L-1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol·L-1醋酸溶液中,充分反应。回答下列问题。(忽略溶液体积的变化)
①如果溶液pH=7,此时V的取值_____20.00(填“>”、“<”或“=”),而溶液中c(Na+)、c(CH3COO-)、c(H+)、c(OH-)的大小关系为_____________________________________________。
②如果V=40.00,则此时溶液中c(OH-) - c(H+) - c(CH3COOH)= ___________________mol·L-1。
化合反应是中学化学中最基本的反应类型之一。请写出三个化合反应的方程式:单质(1)+ 单质(2)= 化合物
所写方程式满足以下要求:①都是短周期元素;
②6种单质分别属于6个不同的主族。
(1);
(2);
(3)。