下列可逆反应达平衡状态后,降温可以使混和气体平均相对分子质量减小的是
A.H2(气)+Br2(气)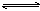 2HBr(气) (正反应为放热反应) 2HBr(气) (正反应为放热反应) |
B.N2(气)+3H2(气)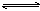 2NH3(气) (正反应为放热反应) 2NH3(气) (正反应为放热反应) |
C.2SO3(气)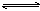 2SO2(气)+O2(气) (正反应为吸热反应) 2SO2(气)+O2(气) (正反应为吸热反应) |
D.4NH3(气)+5O2(气)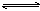 4NO(气)+6H2O(气) (正反应为放热反应) 4NO(气)+6H2O(气) (正反应为放热反应) |
对于可逆反应A(g)+2B(g)  C(g) ΔH<0,下列“研究目的”和“图示”相符的是
C(g) ΔH<0,下列“研究目的”和“图示”相符的是
| 选项 |
A |
B |
C |
D |
| 研究 目的 |
压强对反应的 影响(P2>P1) |
温度对反应的影响 |
平衡体系增加A 对反应的影响 |
催化剂对反应的影响 |
| 图示 |
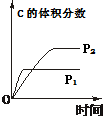 |
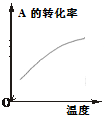 |
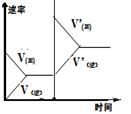 |
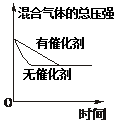 |
下列事实能说明H2SO3不是强电解质的是
① 0.05 mol/L H2SO3 溶液的pH>1 ,②常温下Na2SO3溶液的pH>7 ,
③ H2SO3不稳定,易分解,④H2SO3能与碳酸钠反应制CO2 ,
⑤ H2SO3能和水以任意比例互溶,⑥ 1mol H2SO3能够消耗2 mol NaOH
| A.①②⑤ | B.①②④ | C.①②③⑤ | D.①② |
下列关于平衡常数的说法中,正确的是
| A.化学平衡常数用来定量描述化学反应的限度 |
| B.利用化学平衡常数判断化学反应进行的快慢 |
| C.平衡常数的大小与温度、浓度、压强、催化剂有关 |
| D.对于一个化学反应达到平衡之后,若只改变一个因素使得平衡发生移动,则K值一定变化 |
下列说法正确的是
| A.有气体参加的化学反应,若增大压强,可增加活化分子的百分数,从而使反应速率增大 |
| B.增大反应物浓度,可增大活化分子的百分数,从而使单位时间内有效碰撞次数增多 |
| C.在化学反应中,加入催化剂只能增大正反应速率 |
| D.升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数 |
对于反应4CO(g)+2NO2(g)  N2(g)+4CO2(g),以下化学反应速率的表示中,所表示反应速率最快的是
N2(g)+4CO2(g),以下化学反应速率的表示中,所表示反应速率最快的是
| A.v(CO)=1.6 mol·(L·min) -1 | B.v(NO2)=0.9 mol·(L·min) -1 |
| C.v(N2)=0.25mol·(L·min) -1 | D.v(CO2)=1.2 mol·(L·min) -1 |