在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g) 
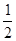 N2(g)+CO2(g);ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g)+CO2(g);ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 | D.降低温度同时增大压强 |
下列各组离子,在强酸性溶液中可以大量共存的是
| A.K+、Na+、NO3-、SiO32- | B.K+、Na+、Ba2+、SO42- |
| C.K+、Ca2+、Na+、CO32﹣ | D.H+、NH4+、K+、Cl- |
下列各组中的两物质相互反应时,与反应条件和用量无关的是
| A.Na和O2 | B.Fe和FeCl3 |
| C.CO2和NaOH | D.AlCl3和NaOH |
下列物质中,既能和酸反应又能和碱反应的化合物是
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3
| A.②③④ | B.①②④ | C.①②③④ | D.①③④ |
除去NaCl溶液中混有的Ca2+、Mg2+、SO42-、HCO3-等杂质,通常采用以下四种试剂:①Na2CO3 ②BaCl2 ③NaOH ④盐酸,加入试剂顺序合理的是
| A.④②①③ | B.①③②④ | C.③②①④ | D.①②③④ |
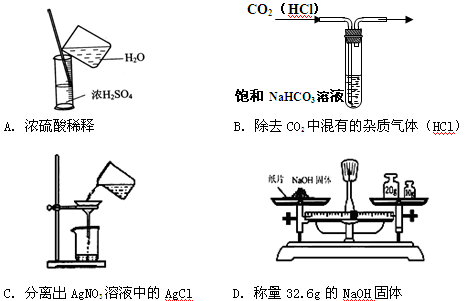
实验是研究化学的基础,下图中所示的实验方法、装置或操作均正确的是