一定条件下,向2 L容积不变的密闭容器中加入一定量的N2、H2和NH3三种气体,发生反应:2NH3(g)  N2(g)+3H2(g)(ΔH>0),各物质的浓度随时间的变化如图1所示。图2为t2时刻后改变容器内的某一条件,反应速率(v)随时间(t)的变化情况。
N2(g)+3H2(g)(ΔH>0),各物质的浓度随时间的变化如图1所示。图2为t2时刻后改变容器内的某一条件,反应速率(v)随时间(t)的变化情况。
下列叙述正确的是( )
| A.若容器内气体的密度不再发生变化,则说明反应达到平衡状态 |
| B.若t1=20 s,则从t0~t1内的平均反应速率v(NH3)=0.01 mol·L-1·s-1 |
| C.图2中,t2时改变的条件是降低温度,t3时改变的条件是增大压强 |
| D.若t2时,再向容器中加入1.4 mol NH3、0.8 mol H2,则平衡将正向移动 |
上海磁悬浮铁路是世界上第一条投入运营的商业磁悬浮铁路。磁悬浮的核心技术是利用超导体的反磁性。以Y2O3、BaCO3和CuO为原料,经研磨烧结可合成一种高温超导物质YBa2Cu3Ox。现欲合成0.5mol此高温超导物质,理论上需取Y2O3、BaCO3和CuO的物质的量分别为
| A.0.50、0.50、0.50 | B.0.50、1.0、1.5 |
| C.0.25、1.0、1.5 | D.1.0、0.25、0.17 |
如果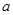 g某气体中含有的分子数为
g某气体中含有的分子数为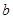 ,则
,则 g该气体在标准状况下占有的体积应表示为(式中
g该气体在标准状况下占有的体积应表示为(式中 为阿伏加德罗常数)
为阿伏加德罗常数)
A. |
B.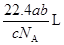 |
C.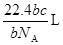 |
D.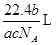 |
CO和H2的混和气体的摩尔质量为8.5 g/mol,则此混和气体中CO和H2的物质的量之比是:
| A.1:3 | B.3:1 | C.1:14 | D.14:1 |
同温同压下,甲、乙两容器分别盛有CH4和NH3,已知它们所含氢原子个数相同,则甲、乙两容器的体积比为
| A.4∶3 | B.5∶4 | C.4∶5 | D.3∶4 |
在溶液中能大量共存,加入OH—有沉淀析出,加入H+有气体放出的是
| A.Na+、Cu2+、Cl—、SO42— | B.Fe3+、K+、SO42—、NO3— |
| C.H+、Al3+、OH—、NO3— | D.Na+、Ca2+、Cl—、HCO3— |