(原创)含氮化合物对人类生活有十分重大的意义。
(1)目前广泛使用的工业合成氨方法是用氮气和氢气在一定条件下化合。
已知:N2(g)+O2(g) =2NO(g) △H=+180.5kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-905kJ/mol
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
①写出工业合成氨的热化学方程式: 。
②实验室模拟合成氨,在2L密闭容器中投入1molN2 和3mol H2,容器中氨气的体积分数随时间变化如图所示。则0~10min,NH3的平均速率为 ;达平衡时,N2的转化率为 。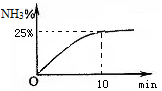
③若在②达平衡后,保持容器体积及温度不变,移走0.5molNH3,再达平衡时,N2的体积分数将 ,平衡常数 (填“增大”“减小”或“不变”)
(2)科学家一直致力于研究常温常压下“人工固氮”的方法。据报道:在常温常压条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水反应,生成NH3和一种单质。进一步研究NH3生成量与温度关系,部分实验数据如下(反应时间3h,其余条件一样)
| T/℃ |
30 |
40 |
50 |
| NH3生成量/10-6mol |
4.8 |
5.9 |
6.0 |
①写出常温下“人工固氮”反应的化学方程式:
此反应△H 0(填“>”、“<”或“=)。
②该反应中的催化剂TiO2的制取方法之一是将TiCl4气体导入氢氧火焰中(700~1000℃)进行水解。写出TiCl4水解的化学方程式:
③在上述固氮过程中,除加入催化剂外,能提高生产速率,但不降低产率的措施还可以是 。
A.适当升高温度 B.将氨气液化分离
C.增大反应物N2的浓度 D.增大压强
(1)请将下列五种物质:KBr、Br2、I2、KI、K2SO4分别填入下列横线上,组成一个未配平的化学方程式:
KBrO3+________+H2SO4―→________+________+________+________+H2O。
(2)如果该化学方程式中I2和KBr的化学计量数分别是8和1,则
①Br2的化学计量数是________;
②请将反应物的化学式及配平后的化学计量数填入下列相应的位置中:
________KBrO3+________+________H2SO4―→……;
③若转移10 mol电子,则反应后生成I2的物质的量为________。
常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH4+、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO3—、SO42—、CO32—,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题。
(1)五种盐中,一定没有的阳离子是____________;所含阴离子相同的两种盐的化学式是________________。
(2)D的化学式为______________,D溶液显碱性的原因是(用离子方程式表示)__________________________________________。
(3)A和C的溶液反应的离子方程式是_________________________;E和氨水反应的离子方程式是____________________。
(4)若要检验B中所含的阳离子,正确的实验方法是________________。
已知有机物A、B、C、D、E、F、G有如下转化关系,其中C的产量可用来衡量一个国家的石油化工发展水平,G的分子式为C9H10O2,试回答下列有关问题。
(1)G的结构简式为 。
(2)指出下列反应的反应类型:A转化为B: ,C转化为D: 。
(3)写出下列反应的化学方程式:
D生成E的化学方程式: 。
B与F生成G的化学方程式: 。
(4)符合下列条件的G的同分异构体有 种:①苯环上有3个取代基,且有两个取代基相同;②能够与新制的银氨溶液反应产生银镜。其中氢原子共有四种不同环境的所有物质的结构简式为 、 。
从樟科植物枝叶提取的精油中含有下列甲、乙、丙三种成分:
(甲)
| 分子式 |
C9H8O |
| 部分性质 |
能使Br2/CCl4褪色 |
(乙)
| 分子式 |
C16H14O2 |
| 部分性质 |
能使Br2/CCl4褪色 |
| 能在稀硫酸中水解 |
(丙)
(1)甲中所含官能团的名称为 、 。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
甲
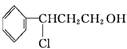
 Y
Y 乙
乙
其中反应Ⅰ的反应类型为 ,反应Ⅰ的目的是 。
(3)已知:
RCH CHR'
CHR' RCHO+R'CHO;2HCHO
RCHO+R'CHO;2HCHO HCOOH+CH3OH
HCOOH+CH3OH
由乙制丙的一种合成路线图如下(A~F均为有机物,图中Mr表示相对分子质量):
①下列物质不能与C反应的是 (选填序号)。
A.金属钠 B.HBr C.Na2CO3溶液 D.乙酸
②写出由E生成F的反应方程式: 。
③D有多种同分异构体,写出其中一种能同时满足下列条件的异构体结构简式 。
a.苯环上连接着三种不同官能团
b.能发生银镜反应
c.能与Br2/CCl4发生加成反应
d.遇FeCl3溶液显示特征颜色
④写出丙的结构简式: 。
甜樱桃中含有一种羟基酸(用A表示),A的碳链结构无支链,分子式为C4H6O5,1.34 g A与足量NaHCO3溶液反应,生成标准状况下的气体0.448 L。A在一定条件下可发生如下转化:
A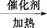 B
B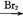 C
C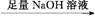 D
D E
E
其中,E的分子式为C4H6O6。已知: +
+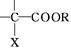

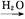
 +Zn(OH)X
+Zn(OH)X
(X代表卤原子,R代表烃基),A的合成方法如下:
①F+BrCH2—COOCH2CH3
 G+Zn(OH)Br
G+Zn(OH)Br
②G+2H2O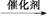 A+2M(其中,F、G、M分别代表一种有机物)
A+2M(其中,F、G、M分别代表一种有机物)
请回答下列问题:
(1)E的结构简式为 ,E的核磁共振氢谱中会出现 组峰,一分子E最多能与 分子乙醇发生分子间脱水反应。
(2)从A到D所发生的化学反应的类型依次是 。
(3)F的分子式是 。写出满足下列条件的F的同分异构体的结构简式:①能与NaHCO3反应,且常温下能使溴水褪色;②不能发生银镜反应;③1 mol该同分异构体与足量钠反应,标准状况下可得到22.4 L氢气(注:羟基不能直接与双键相连)。
(4)写出G与水反应生成A和M的化学方程式 。