X、Y、Z是原子序数依次增大且属于不同周期的三种常见短周期元素,三种元素相互之间可以形成1:1型的化合物M、N、R,常温下M、N为固体,R为液体.M、N遇到水都能产生气体,而且产生的气体相互可以化合,下列说法正确的是
| A.三种元素都是非金属元素 | B.Z是地壳中含量最多的元素 |
| C.三种化合物都是共价化合物 | D.M、N投入水中所得溶液中溶质相同 |
现有5种短周期元素X、Y、Z、Q、W,原子序数依次增大,在周期表中X原子半径最小;X和W同主族;Y元素原子核外电子总数是其次外层电子数的3倍;Q元素是地壳中含量最高的元素。下列说法不正确的是
| A.原子半径:Y<Q<W |
| B.ZX3可使紫色石蕊溶液变蓝 |
| C.X、Z、Q3种元素可组成离子化合物或共价化合物 |
| D.X2Q2、Y2X62种分子中含有的电子数、化学键种类都相同 |
已知A、B、C、D四种短周期元素,A、D同周期,B、C同主族,简单离子A+、D3+、B2-核外电子排布相同,则下列说法不正确的是
A.A、C、D三种元素最高价氧化物对应的水化物能两两反应
B.离子半径大小:B>A>D>C
C.气态氢化物的稳定性B>C
D.A、B、C三种元素组成的化合物中含有离子键和共价键
下图是元素周期表前四周期的一部分,关于元素X、Y、Z的叙述正确的是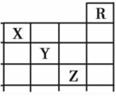
①X的气态氢化物与Y最高价氧化物对应的水化物能发生反应生成盐
②等物质的量浓度的X、Y、Z的气态氢化物的水溶液的pH:X>Y>Z
③Z的单质常温下是液体,一定条件下可与铁粉反应
④Z的原子序数比Y大1 9
⑤Z所在的周期中含有32种元素。
| A.只有③ | B.只有①④ | C.只有①②③④ | D.①②③④⑤ |
M、X、Y、Z是四种常见的短周期元素,各元素在周期表中的位置如图所示,其中只有M属于金属元素。下列说法中,错误的是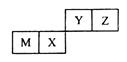
| A.Y元素气态氢化物的稳定性大于Z元素的 |
| B.M和Y两种元素,可以形成电子层结构相同的两种简单离子 |
| C.X元素最高价氧化物对应水化物的酸性弱于Y元素的 |
| D.M元素的氧化物既可以与酸溶液反应,也可以与碱溶液反应 |
短周期元素W、X、Y和Z的原子序数依次增大。元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是
| A.元素W、X的氯化物中,各原子均满足8电子的稳定结构 |
| B.元素X与氢形成的原子比为1:1的化合物有很多种 |
| C.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 |
| D.元素Z可与元素X形成共价化合物XZ2 |