下列工业生产所涉及的化学用语表达不正确是( )
A.工业上制取氯气:MnO2+4HCl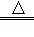 Cl2↑+MnCl2+H2O Cl2↑+MnCl2+H2O |
B.工业上合成氨:N2+3H2  2NH3 2NH3 |
C.工业上制取粗硅:SiO2+2C Si+2CO↑ Si+2CO↑ |
| D.工业上生产漂白粉:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O |
有关晶体的叙述正确的是()
| A.在SiO2晶体中,由Si、O构成的最小单元环是8元环 |
| B.在12g金刚石中,含C—C共价键键数为4NA个 |
| C.在60g二氧化硅中,含Si2O共价键键数为4NA个 |
| D.在NaCl晶体中,与Na+最近且距离相等的Na+有6个 |
根据下列实验事实,能确定某晶体一定是离子晶体的是()
| A.晶体熔点达2500℃ | B.晶体不导电,溶于水导电 |
| C.晶体不导电,熔融能导电 | D.温度越高,溶解度越大 |
下列关予溶液和胶体的叙述,正确的是()
| A.溶液是电中性的,胶体是带电的 |
| B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一级移动 |
| C.溶液中溶质分子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 |
| D.一束光线分别通过溶液和胶体对,后者会出现明显的光带,前者则没有 |
用铂作电极电解500 mL含KNO3和Cu(NO3)2的混合蒲液一段时向后,在两极均生成11.2L标准状况下的气体,原溶液中Cu2+的物质的量浓度为()
| A.0.5 mol/L | B.1 mol/L | C.2 mol/L | D.无法确定 |
把分别盛有熔融的KCl、MgCl2、Al2O3的三个电解槽串联,在一一定条件下通电一段时间后,析出K.Mg.Al的物质的量之比为()
| A.l:2:3 | B.3:2-1 | C.6:3:1 | D.6:3:2 |