铝是自然界中含量最高的金属元素,以铝土矿(主要成分为Al2O3,还含有Fe2O3、SiO2)为原料通过以下途径制备氯化铝晶体:

(1)X是__________(填名称)。
(2)已知Y是氧化铝,目的是调节溶液的pH,根据下表数据,溶液的pH应保持在_______范围。
| |
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
| Fe3+ |
1.9 |
3.2 |
| Al3+ |
4.0 |
5.2 |
(3)检验滤液C中既不存在Fe2+又不存在Fe3+的操作步骤是: (注明试剂、现象)。
(4)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为 (填代号)。

(5)离子液体是一种室温熔融盐,为非水体系,由有机阳离子、Al2Cl7-和AlCl4-组成的离子液体作电解液时,可在钢制品上电镀铝。电镀是钢制品应接电源的 极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为 。不用AlCl3水溶液作电解液的原因是 。
向10ml0.1mol/l的Na[Al(OH)4]溶液中滴加0.1mol/l的HCl溶液,生成沉淀的量与加入的盐酸体积的关系如图
(1)写出OA段的离子方程式
(2)写出AB段的化学方程式
(3)OB段反应共消耗ml盐酸溶液;
此过程中生成沉淀最多时,沉淀物质的量是mol,此时消耗的盐酸是ml
(10分)⑴键线式 表示的分子式;名称是。
表示的分子式;名称是。
⑵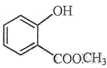 中含有的官能团的名称为
中含有的官能团的名称为
⑶丁基的4个结构简式为________________________________________________________
⑷含有杂质的工业乙醇的蒸馏装置中,玻璃仪器有酒精灯、蒸馏瓶、_______ __、_________、尾接管、锥形瓶
写出支链上共含有3个C原子,主链上含碳原子数最少的烯烃的结构简式。
下列各化合物中,属于同系物的是,属于同分异构体的是(填入编号)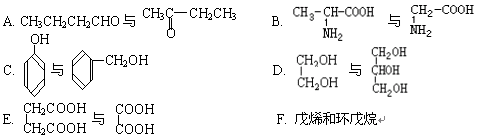
已知有机物A分子中有3个碳原子,有关它的某些信息注明在下面的示意图中: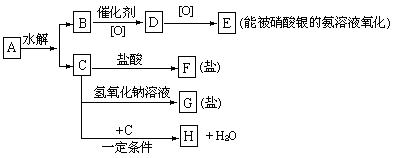
(1 )A、F、G的结构简式为:___________,____________,______________.
(2) 生成H的化学方程式为:__________________________________.