已知黄钠铁矾[NaxFey(SO4)m(OH)n]具有沉淀颗粒大、沉淀速率快、容易过滤等特点。某研究小组先将某废水中Fe2+氧化为Fe3+,再加入Na2SO4使其生成黄钠铁矾而除去。该小组为测定黄钠铁矾的组成,进行了如下实验:
①称取4.850 g样品,加盐酸完全溶解后,配成100.00 mL溶液;
②量取25.00 mL溶液,加入足量的KI,用0.2500 mol·L-1Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00 mLNa2S2O3溶液至终点。
③另取25.00 mL溶液,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥后得沉淀1.165 g。
(1)NaxFey(SO4)m(OH)n中x、y、m、n的代数关系式为 。
(2)用Na2S2O3溶液进行滴定时,使用的指示剂为 ,滴定到终点的颜色变化为 。
(3)通过计算确定黄钠铁矾的化学式(写出计算过程)。
A为两种固体的混合物,G和I为溶液D的组成成分,E为红褐色沉淀,J为淡黄色固体。反应所加的试剂均足量。
(1)混合物A一定含有的元素为(写元素符号);
(2)溶液F一定含有的阴离子为(写离子符号);
(3)写出B+G―→J的化学方程式:
写出溶液C―→溶液D的离子方程式:;
(4)I溶液I中溶质的阳离子常作净水剂,其作用原理是(用离子方程式表示):
。
(8分)有一无色透明澄清溶液,可能含有较大量的Cu2+、Ba2+、SO、NO、
I-、S2-、H+、K+等离子中两种或多种,做如下实验:
①取溶液少量加入铁粉有气体放出;
②另取原溶液加Na2SO3溶液后有气体放出,也有白色沉淀生成,再加盐酸沉淀不完全消失;
③另取原溶液加入AgNO3溶液无沉淀生成。
(1)由此判断原溶液中一定含有的离子是,一定不含有的离子是,可能含有的离子是;
(2)有关反应①的离子方程式为。
已知:①MnO4— +e- MnO42―(绿色)(强碱性条件)
MnO42―(绿色)(强碱性条件)
②MnO4—+ 8H+ + 5e- Mn2+(无色)+ 4H2O(强酸性条件)
Mn2+(无色)+ 4H2O(强酸性条件)
(1)在KOH溶液中,KMnO4与K2SO3溶液发生反应, 写出反应的离子方程式。
(2)将KMnO4溶液滴入NaOH溶液微热,得到透明的绿色溶液,写出反应的离子方程式.
(3)用酸性KMnO4溶液与亚铁盐的反应证明Fe2+具有还原性,MnO4‑具有氧化性,最合适的亚铁盐是(选填编号),可用来酸化KMnO4溶液的试剂是(选填编号)
a. FeCl2 b. FeSO4 c.Fe(NO3)2 d稀硫酸 e. 盐酸 f. 硝酸
(4)向20 mL浓度为0.05mol/L的KMnO4溶液中滴加FeSO4溶液,使MnO4‑全部转化为Mn2+ ,则反应前需向KMnO4溶液加入c(H+)=1mol/L的酸不少于mL
现有A、B、C、D、E、F六种化合物,已知它们的阳离子有K+、Ag+、Ca2+、Ba2+、Fe2+、Al3+,阴离子有Cl-、OH-、CH3COO-、NO 、SO42-、CO32-,六种化合物的阴阳离子均不相同,且均易溶于水。现将它们分别配成0.1 mol·L-1的溶液,进行如下实验:
、SO42-、CO32-,六种化合物的阴阳离子均不相同,且均易溶于水。现将它们分别配成0.1 mol·L-1的溶液,进行如下实验:
①测得溶液A、C、E呈碱性,且碱性为A>E>C;
②向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③向D溶液中滴加Ba(NO3)2溶液,无明显现象;
④向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
根据上述实验现象,回答下列问题:
写出下列六种化合物的化学式:
A、B、C、D、E、F。
甲、乙、丙为短周期常见的单质,乙、丙两元素的原子序数相差8。X、A、B、C、D、E、F、G均为常见的化合物,其中A、G的焰色反应为黄色,A和X的摩尔质量相同。在一定条件下,各物质相互转化关系如下图。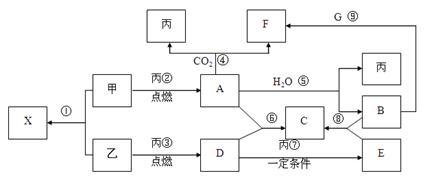
请回答:
(1) 写化学式:X,CD。
(2)写出反应④、⑤的化学反应方程式:④;
⑤
(3)写出反应⑧、⑨的离子方程式⑧
⑨。
(4)在上图的反应中,不属于氧化还原反应的是(填序号)。