2013年11月江苏在大部分地市推广使用含硫量大幅减少的苏V汽油。下列有关汽油的说法正确的是
| A.汽油属于可再生能源 |
| B.将原油通过分馏、裂化可获得汽油 |
| C.苏V汽油是清洁能源,不产生污染 |
| D.苏V汽油不能降低酸雨发生 |
下列溶液中微粒的物质的量浓度关系正确的是()
| A.25℃时,0.1mol/L pH=4.5的NaHC2O4溶液: c(HC2O4-)>c(H2 C2O4)>c(C2O42-) |
| B.NaHCO3溶液:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| C.25℃时,pH=9、浓度均为0.1mol/L的NH3·H2O 、NH4Cl混合溶液: c(NH4+)+(H+)>c(NH3·H2O)+c(OH-) |
| D.0.1mol/L(NH4)2Fe(SO4)2溶液中: |
c(SO42-)=c(NH4+)>c(Fe2+)>c(H+)>c(OH-)
X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物。下表各组物质之间通过一步反应不能实现如图所示转化的是()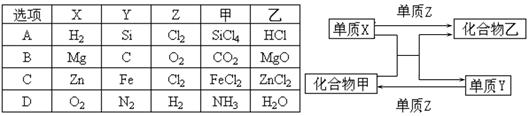
下列装置或操作不能达到实验目的的是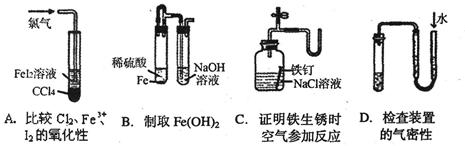
用NA表示阿伏加德罗常数的值。下列叙述正确的是()
| A.3.6 g碳与3.36 L O2一定条件下恰好完全反应,生成CO分子数一定为0.3NA |
| B.6.9 g钠与足量的CO2和H2O (g)混合气体充分反应,转移的电子数一定为0.3NA |
| C.25℃时, 0.15mol/L的Na2CO3溶液中,Na+数目为0.3NA |
| D.标准状况下,2.24L氯仿中含有C-Cl数目为0.3NA |
下列化学用语表示正确的是()
A.NaH与重水反应的方程式:NaH+D2O=NaOH+D2↑ |
B.三氟化氮的电子式: |
| C.熔融状态下硫酸氢钠的电离方程式:NaHSO4(熔融)=Na++HSO4- | |
D.质量数为137的钡原子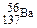 |