向甲、乙两恒温恒容的密闭容器中,分别充入一定量的A和B,发生反应:A(g)+B(g)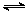 xC(g)+D(s) △H<0。测得两容器中c(A)随时间t的变化如图所示:
xC(g)+D(s) △H<0。测得两容器中c(A)随时间t的变化如图所示:

| 容器 |
甲 |
乙 |
| 容积(L) |
1 |
1 |
| 反应放热(kJ) |
a |
b |
| 反应物起始量 |
2 molA、2 molB |
1 molA、1 molB |
下列说法不正确的是
A.x=1
B.该温度下反应的平衡常数K=4
C.a=2b
D.保持其他条件不变,起始时向乙容器充入0.2 mol A、0.4 mol B、0.4 mol C、0.8molD,则此时v(正)> v(逆)
用惰性电极电解含有0.1molNaCl与0.1molCuSO4的溶液0.5L,此过程中当转移了0.3mol电子时,阳极上析出的气体总共为
| A.0.05 mol | B.0.075mol |
| C.0.1 mol | D.0.125 mol |
1mol 与足量的NaOH溶液充分反应,最多能消耗NaOH的物质的量为
与足量的NaOH溶液充分反应,最多能消耗NaOH的物质的量为
| A.2 mol | B.3 mol |
| C.4 mol | D.5 mol |
在FeS2+ O2 → Fe2O3+ SO2反应中,还原剂与还原产物的物质的量之比为
| A.2:5 | B.1:4 |
| C.2:1 | D.1:2 |
下列叙述正确的是
| A.同族元素的氢化物的沸点随相对分子质量的增加而递增 |
| B.干冰晶体中的作用力只存在分子之间作用力 |
| C.碱金属的单质的沸点随相对原子质量的增加而递降 |
| D.向碳酸钠溶液中通入过量的二氧化碳,溶液会变浑浊 |
在溶液中能大量共存的离子组是
| A.Ba2+、HSO4-、Cl-、NO3- | B.Fe3+、NH4+、SCN-、OH- |
| C.OH-、Ag(NH3)2+、Na+、K + | D.HS-、Na+、ClO-、Fe2+ |