铝和镓的性质相似,如M(OH)3都是难溶的两性氢氧化物。在自然界镓常以极少量分散于铝矿中。用NaOH溶液处理铝矿(Al2O3)时,生成NaAlO2、NaGaO2;而后通入适量CO2,得Al(OH)3沉淀,而NaGaO2留在溶液中(循环多次后成为提取镓的原料)。发生后一步反应是因为
| A.铝酸酸性弱于镓酸 | B.铝酸酸性强于镓酸 |
| C.NaGaO2浓度小,不沉淀 | D.Al(OH)3是难溶物 |
关于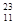 Na+,下面的叙述中正确的是( )
Na+,下面的叙述中正确的是( )
| A.质子数为11 | B.电子数为11 | C.中子数为11 | D.质量数为11 |
容量瓶上需标有以下六项中的()A
①温度②浓度③容量④压强⑤刻度线⑥酸式或碱式
| A.①③⑤ | B.③⑤⑥ | C.①②④ | D.②④⑥ |
若NA表示阿伏加德罗常数,下列关于0.3mol /L的MgCl2溶液的说法正确的是()
| A.100毫升的溶液中含有Mg2+、Cl-—总数为0.3NA |
| B.100毫升的溶液中含有Mg2+数目是0.1NA |
| C.1升溶液中Mg2+的浓度是0.3mol / L |
| D.1.5升溶液中含有Cl-的浓度是4.5mol / L |
用于配制一定物质的量浓度的溶液的实验装置是: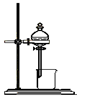
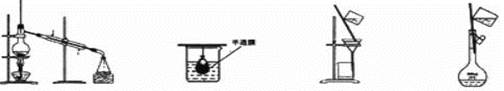
A B C D
检验溶液中是否含有Cl-,选用的试剂是稀硝酸和AgNO3溶液,其中稀硝酸的作用是()
| A.加速反应的进行 | B.排除某些杂质离子的干扰 |
| C.生成不溶于水的物质 | D.加大沉淀的生成量 |