下列判断错误的是( )
| A.酸性:HClO4>H2SO4>H3PO4 | B.沸点:NH3>PH3>AsH3 |
| C.熔点:Si3N4>NaCl>SiI4 | D.碱性:NaOH>Mg(OH)2>Al(OH)3 |
为测定某有机物的结构,用核磁共振仪处理后得到如图所示的核磁共振氢谱,则该有机物可能是 ()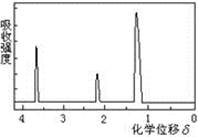
| A.C2H5OH | B. |
| C.CH3CH2CH2COOH | D.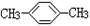 |
下列实验或操作能达到实验目的的是()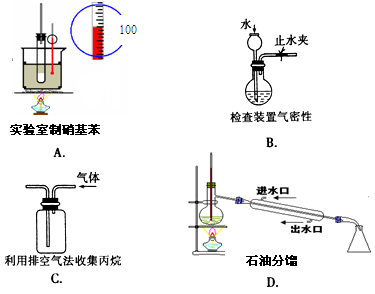
下列有机化合物中均含有酸性杂质,除去这些杂质的方法中正确的是()
| A.苯中含苯酚杂质:加入溴水,过滤 |
| B.乙醇中含乙酸杂质:加入碳酸钠溶液洗涤,分液 |
| C.乙醛中含乙酸杂质:加入氢氧化钠溶液洗涤,分液 |
| D.乙酸丁酯中含乙酸杂质:加入碳酸钠溶液洗涤,分液 |
下列说法不正确的是()
| A.麦芽糖及其水解产物均能发生银镜反应 |
| B.用溴水即可鉴别苯酚溶液、2,4己二烯和甲苯 |
| C.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
D.用甘氨酸( )和丙氨酸( )和丙氨酸(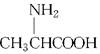 )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 |
根据有机化合物的命名原则,下列命名正确的是()
A. 3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 |
B. 2-羟基丁烷 2-羟基丁烷 |
| C.CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 |
| D.CH3CH(NH2)CH2COOH 3-氨基丁酸 |