脱水环化是合成生物碱类天然产物的重要步骤,某生物碱合成路线如下: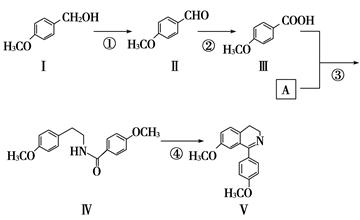
(1)化合物Ⅱ的化学式为________。
(2)反应①的化学方程式为(不要求写出反应条件)______________________________________。
(3)化合物A的结构简式为____________。
(4)下列说法正确的是______________。
| A.化合物Ⅱ能发生银镜反应 |
| B.化合物Ⅰ~Ⅴ均属于芳香烃 |
| C.反应③属于酯化反应 |
| D.1 mol化合物Ⅱ能与4 mol H2发生加成反应 |
E.化合物Ⅰ、Ⅱ、Ⅲ均能与金属钠反应放出氢气
(5)化合物Ⅵ与化合物Ⅲ互为同分异构体,Ⅵ中含有酯基,且能与FeCl3溶液发生显色反应,其苯环上的一氯代物只有2种。写出一种满足上述条件的Ⅵ的结构简式:______________。
(6)化合物Ⅶ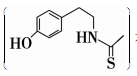 在一定条件下也能发生类似上述第④步骤的环化反应,化合物Ⅶ环化反应产物的结构简式为____________。
在一定条件下也能发生类似上述第④步骤的环化反应,化合物Ⅶ环化反应产物的结构简式为____________。
位于短周期的四种元素a、b、c、d、e,原子序数依次增大,已知a的单质最轻,d是地壳中含量最多的金属元素,a和d的原子序数之和等于b的原子序数的两倍,e的质子数是c的两倍且同主族。据此回答下列问题
(1)d元素在周期表中的位置 。
(2)有a和b元素组成的四核10电子分子的电子式 。实验室制取该种物质的化学方程式为 。
(3)写出由a和c两种元素形成的18电子的物质的结构式 ,往一定量的氯化亚铁溶液中滴加适量该物质溶液,发生反应的离子方程式为 。
(4)由d和e两种元素组成的化合物投入水中所观察到的现象 ,该过程的化学反应方程式为 。
如图是有关物质相互转化的关系图,其中A俗称铁红,甲为强酸,乙为还原性气体,丙为强碱溶液,G为红褐色沉淀,I的颜色呈浅绿色。
(1)若F是由Na+和SO42﹣组成的溶液,则甲的化学式是 ,列举A物质的一种用途 。
(2)若D是能使澄清石灰水变浑浊的气体,则乙的化学式为 ,丁属于单质、酸、碱中的 ;在I溶液中加入氢氧化钠溶液,可以观察到的现象是 ,对应的离子方程式和化学方程式依次是 。
(3)写出G→A+C的化学方程式: 。
(4)写出E和C反应的方程式并用单线桥法标明电子的转移方向和数目: 。
(5)若A中混有杂质Al2O3,除去杂质的方法是加入过量的NaOH溶液,该反应的离子方程式为。
(6)由E和A组成的混合物与稀H2SO4作用,固体恰好溶解,所得溶液中不含Fe3+,且生成的Fe2+与H2的物质的量之比为4:1.则反应物中A、E、H2SO4的物质的量之比为 。
现有A、B、C、D、E、F、G、H、I九种物质,其中A、B、C均为氧化物,且A为淡黄色粉末,I、E为气体单质,它们之间相互关系如图,其他与题无关的生成物均已略去。请回答下列问题:
(1)写出化学式:
A ,G ,H 。
(2)写出下列反应的离子方程式“
A+B → D+E
F+Ca(OH)2→ D
D+I→ G
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。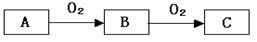
(1)若A是一种黄色单质固体,则B→C的化学方程式为 。
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为 。将C长期露置于空气中,最后将变成物质D。现有D和NaHCO3的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38 g,D的质量分数为 。
(3)若C是红棕色气体,A可能是一种能用下图装置制取的气体,请结合所学知识,回答下列问题:
①写出实验室制取A的化学方程式 。
②收集A的方法是 ,验证A是否已经收集满的方法是:
(任写一种)。
③若有5.35g氯化铵参加反应,则产生的A气体在标准状况下的体积为 L。
现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,其中A在常温下能与水发生剧烈反应,B是目前使用最多的金属。物质之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:乙 ; F ;
(2)写出下列反应的离子方程式:
①金属A和水反应的离子方程式 。
②D和G的水溶液反应的离子方程式 。
(3)将G浓溶液逐滴加入到沸水中会产生一种红褐色的液体。你认为该液体中的分散质粒子直径在 之间,验证的简单方法是: 。