下列离子方程式书写正确的是
| A.将少量的H2S气体通入硫酸铜溶液中: H2S+Cu2+=CuS↓+2H+ |
| B.将NO2气体通入水中:2NO2+H2O= NO3-+ NO↑+2H+ |
| C.ICl 和Cl2的化学性质相似,将ICl通入KOH溶液中:ICl+2OH-=I-+ ClO-+H2O |
| D.往100ml 1.5mol/L的FeBr2溶液中通入0.15mol Cl2:2Br-+Cl2=Br2+2Cl- |
运用有关概念判断下列叙述正确的是
| A.1molH2燃烧放出的热量为H2的燃烧热 |
| B.Na2SO3和H2O2的反应为氧化还原反应 |
C.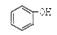 和 和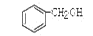 互为同系物 互为同系物 |
| D.BaSO4的水溶液不导电,故BaSO4是弱电解质 |
现有Fe2O3和Fe3O4组成的混合物W g,将其投入到V mL5mol/L的盐酸中,再加入22.4g铁粉,固体恰好完全溶解,收集到标准状况下气体4480mL。向反应后溶液中滴加KSCN溶液,无颜色变化,下列推断正确的是
| A.转移电子为1.0mol | B.W可能等于48.8 |
| C.V可能等于360 | D.发生的反应均为氧化还原反应 |
下列几组标签被腐蚀的试剂①Al2(SO4)3溶液、KOH溶液②NaAlO2溶液 、H2SO4溶液③NaHCO3溶液、 HCl溶液④AgNO3、氨水⑤CuSO4溶液、NaOH溶液⑥CCl4、NaCl溶液,不用其他试剂,只用胶头滴管和试管就可以鉴别的是
| A.①②③④ | B.①②④⑤⑥ | C.①②③④⑤ | D.全部 |
下列叙述中,正确的是
A.依据铝热反应原理,能发生反应2Al+3MgO 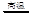 3Mg+Al2O3 3Mg+Al2O3 |
| B.在加入铝粉能放出氢气的溶液中:K+、NH4+、CH3COO-、Cl-一定能够大量共存 |
| C.铁片放入过量的稀硝酸中:3Fe+8H++2NO3-===3Fe2++2NO↑+4H2O |
| D.氯化铝溶液中加入过量氨水反应实质是Al3++3NH3·H2O===Al(OH)3↓+3NH4+ |
某溶液中只可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是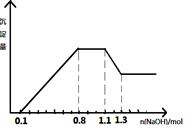
| A.溶液中的阳离子只有H+、Mg2+、Al3+可能含有Fe3+ |
| B.溶液中一定不含CO32-和NO3-,一定含有SO42- |
| C.溶液中c(NH4+)=0.3 mol/L |
| D.c(H+)∶c (Al3+)∶c(Mg2+)=1∶1∶1 |