汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3 =K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断正确的是
| A.生成40.0LN2(标准状况) | B.有0.250molKNO3被氧化 |
| C.转移电子的物质的量为1.25mol | D.被氧化的N原子的物质的量为3.5mol |
下列哪一个分子模型属于球棍模型()
A.苯分子 |
B.水分子 |
C.乙炔分子 |
D.乙烯分子 |
下列关于苯的说法错误的是()
A.苯 通常是无色的液体,不溶于水 通常是无色的液体,不溶于水 |
B.苯分子具 有平面正六边形的结构 有平面正六边形的结构 |
| C.苯分子内部是单双键交替的结构 | D.苯不能与酸性高锰酸钾溶液反应 |
已知乙烯能被酸性高锰酸钾溶液氧化成CO2。既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的少量 乙烯的方法是()
乙烯的方法是()
| A.在空气中燃烧 | B.通入足量溴水中 |
| C.通入酸性高锰酸钾溶液中 | D.通入水中 |
下列物质在一定条件下可与CH4发生取代反应 的是()
的是()
| A.氧气 | B.氯气 | C.溴水 | D.酸性高锰酸钾 |
右图是一种航天器能量储存系统原理示意图。下列说法正确的是()
| A.该系统中只存在3种形式的能量转化 |
B.装置Y中负极的电极反应式为: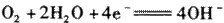 |
| C.装置X能实现燃料电池的燃料和氧化剂再生 |
| D.装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |