常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 0.1000 mol/L盐酸和20.00 mL 0.1000 mol/L醋酸溶液,得到2条滴定曲线,如下图所示: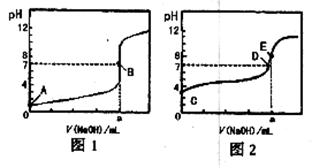
以HA表示酸,下列说法正确的是( )
A.滴定盐酸的曲线是图2
B.达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A—)
C.达到B、E状态时,反应消耗的n( CH3COOH)>n(HCl)
D.当0mL< V(NaOH)<20.00mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A-)>c(Na+)>c(H+)>c(OH-)
将2molS02和2molO2放入一个容器中,在一定的条件下反应到达平衡状态,此时,容器存在的各物质的量中,下列可能存在的是:()
| A.0molS02 | B.2mol S03 | C.1mol 02 | D.1molSO3 |
右图所示是可逆反应X2+3Y2 2Z在 反应过程总中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是()
2Z在 反应过程总中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是()
| A.t1时,只有正向反应 | B.t2时反应达到限度 |
| C.t2-t3时,反应停止 | D.t2-t3时,v(Y2)=v(Z) |
已知在25℃、1.0×105Pa条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是()
| A.H2O(g)==H2(g)+1/2 O2(g) ΔH=+242 kJ·mol-1 |
| B.2H2(g)+O2(g)===2H2O(l) ΔH=-484kJ·mol-1 |
| C.H2(g)+1/2 O2(g)==H2O(l) ΔH=-242kJ·mol-1 |
| D.2H2(g)+O2(g)==2H2O(g) ΔH=+484 kJ·mol-1 |
在密闭容器中进行可逆反应,A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)[mol·(L·s)-1]来表示,且v(A)、v(B)、v(C)之间有以下关系:v(B)=3v(A), 3v(C)=2v(B)。则此反应可表示为 ()
A.2A+3B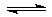 2C B.A+3B
2C B.A+3B 2C
2C
C.3A+B 2C D.A+B
2C D.A+B C
C
下列各组物质中,两者既不是同位素,也不是同素异形体,还不是同分异构体的是()
| A.D和T | B.CH3COOH和HCOOCH3 |
| C.CH4和CH3CH3 | D.金刚石和石墨 |