下列有关实验的说法正确的是( )
| A.实验室配制FeCl3溶液时加入铁粉和稀盐酸 |
| B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量 |
| C.除去铁粉中混有少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 |
| D.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,该溶液中一定含有CO32- |
有机物分子H3C─ ─CH=CH-C≡C-CH3中最多有多少个原子共面
─CH=CH-C≡C-CH3中最多有多少个原子共面
| A.12 | B.16 | C.20 | D.24 |
一定量的某有机物完全燃烧后,将燃烧产物通过足量的石灰水,经过滤 可得沉淀10克,但称量滤液时,其质量只减少2.9克,则此有机物不可能是
可得沉淀10克,但称量滤液时,其质量只减少2.9克,则此有机物不可能是
| A.乙烷 | B.乙烯 | C.乙醇 | D.乙二醇 |
历史上最早应用的还原性染料是靛蓝,其结构简式如图所示。
下列关于靛蓝的叙述中错误的
| A.靛蓝由碳、氢、氧、氮四种元素组成 |
| B.它的分子式是C16H10N2O2 |
| C.该物质是高分子化合物 |
| D.它是不饱和的有机物 |
下列反应的化学方程式(或离子方程式)错误的是
A.苯酚与氢氧化钠溶液反应 —OH + OH —→ —OH + OH —→ —O —+ H2O —O —+ H2O |
B.溴乙烷与NaOH溶液混和共热CH3CH2Br + NaOH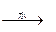 CH2=CH2+H2O+NaBr CH2=CH2+H2O+NaBr |
C.乙醛与银氨溶液反应CH3CHO+2[Ag(NH3)2]OH CH3COONH4+2Ag↓+3NH3+H2O CH3COONH4+2Ag↓+3NH3+H2O |
D.乙醇的消去反应 CH3CH2OH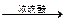 CH2=CH2 ↑+H2O CH2=CH2 ↑+H2O |
某实验小组对甲、乙、丙、丁四种固体样品的性质进行测试,结果如下表:
| 物质 性质 |
甲 |
乙 |
丙 |
丁 |
| 熔点 |
高 |
低 |
高 |
低 |
| 水溶性 |
溶 |
不溶 |
不溶 |
溶 |
| 高温 |
稳定 |
分解 |
稳定 |
稳定 |
| 导电性 |
导电 |
不导电 |
不导电 |
导电 |
则这四种固体物质中最可能是有机物的是
A.甲 B.乙 C.丙 D.丁