FeBr2是一种黄绿色鳞片状的固体,某研究性学习小组为了探究它的还原性,进行了如下实验:
I:实验需要90mL 0.1mol/LFeBr2溶液
(1)配制FeBr2溶液除烧杯、玻璃棒、量筒、胶头滴管外还需的玻璃仪器是
(2)下列有关配制过程中说法正确的是 (填序号)。
a.用托盘天平称量质量为1.94g的FeBr2
b.将称量的FeBr2放入容量瓶中,加90mL蒸馏水溶解
c.洗涤溶解FeBr2的烧杯,并将洗涤液转移至容量瓶中
d.容量瓶贴签存放配好的FeBr2溶液
e.定容时,仰视容量瓶刻度线会使配制的FeBr2溶液浓度偏低
II:探究FeBr2的还原性
取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br- 被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+ 被Cl2氧化成Fe3+。
请你完成下表,验证假设:
| 实验步骤、预期现象 |
结论 |
| ①向溶液中加入适量CCl4,振荡、静置后 现象:__________________________; |
假设1正确 |
| ②向溶液中加入 溶液 现象: 。 |
假设2正确 |
若假设1正确,从实验①中分离出Br2的实验主要操作名称是 ;
(2)实验证明:还原性Fe2+ > Br-
请用一个离子方程式来证明: ;
(3)若在50mL上述FeBr2溶液中通入5×10-3molCl2,则反应的离子方程式为: 。
溴化碘(IBr)的化学性质类似于卤素单质,试完成下列问题:
(1)溴化碘的电子式是__________,它是由__________键形成的__________分子。
(2)溴化碘和水反应生成了一种三原子分子,该分子的电子式为__________。
将几种分子晶体在水和四氯化碳中的溶解情况填入下表(填“易溶”或“不易溶”):
| 蔗糖 |
磷酸 |
碘 |
萘 |
|
| (1)水 |
||||
| (2)四氯化铁 |
其原因是____________________________________________________________。
“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一。有关理论认为N2O与CO2分子具有相似的结构(包括电子式);又已知N2O分子中氧原子只与一个氮原子相连,则N2O的电子式可表示为__________,由此可知它__________ (填“含有”或“不含”)非极性键。
氮可以形成多种离子,如N3-、NH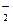 、N
、N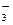 、NH
、NH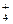 、N2H
、N2H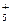 、N2H
、N2H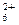 等,已知N2H
等,已知N2H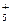 与N2H
与N2H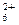 是由中性分子结合质子形成的,类似于NH
是由中性分子结合质子形成的,类似于NH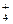 ,因此有类似于NH
,因此有类似于NH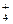 的性质。
的性质。
(1)NH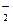 的电子式为__________。
的电子式为__________。
(2)N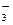 有__________个电子。
有__________个电子。
(3)写出两种由多个原子组成的含有与N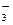 电子数相同的物质的化学式__________。
电子数相同的物质的化学式__________。
(4)等电子数的粒子往往具有相似的结构,试预测N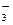 的构型____________________。
的构型____________________。
(5)据报道,美国科学家卡尔·克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。则“N5”分子碎片所带电荷是__________。
W、X、Y、Z四种短周期元素的原子序数X>W>Z>Y。W原子的最外层没有p电子,X原子核外s电子与p电子数之比为1∶1,Y原子最外层s电子与p电子数之比为1∶1,Z原子核外电子中p电子数比Y原子多2个。
(1)X元素的单质与Z、Y所形成的化合物反应,其化学方程式:________________________。
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为__________<__________(用分子式表示)。
(3)这四种元素原子半径的大小为__________>__________>__________>__________(填元素符号)。