为探究NaHCO3、Na2CO3与1mol·L-1盐酸反应(设两反应分别是反应Ⅰ、反应Ⅱ)过程中的热效应,进行实验并测得如下数据:
| 序号 |
液体 |
固体 |
混合前温度 |
混合后最高温度 |
| ① |
35 mL水 |
2.5g NaHCO3 |
20℃ |
18.5℃ |
| ② |
35 mL水 |
3.2g Na2CO3 |
20℃ |
24.3℃ |
| ③ |
35 mL盐酸 |
2.5g NaHCO3 |
20℃ |
16.2℃ |
| ④ |
35 mL盐酸 |
3.2g Na2CO3 |
20℃ |
25.1℃ |
下列有关说法正确的是
A.仅通过实验③即可判断反应Ⅰ是吸热反应
B.仅通过实验④即可判断反应Ⅱ是放热反应
C.通过实验可判断出反应Ⅰ、Ⅱ分别是吸热反应、放热反应
D.通过实验可判断出反应Ⅰ、Ⅱ分别是放热反应、吸热反应
羰基硫(OCS)是一种有臭鸡蛋气味的无色气体,分子结构与CO2相似,高温下分解为CO和S。下列有关说法正确的是()
| A.OCS、CO2、CO、S晶体类型相同 |
| B.OCS高温分解时,碳元素化合价升高 |
| C.OCS中含有1个σ键和1个π键 |
| D.22.4 L OCS中约含有3×6.02× 1023个原子 |
下列物质中,跟溴水、新制的Cu(OH)2悬浊液、Na2CO3、苯酚钠都能起反应的是()
| A.乙醇 | B.乙醛 | C.乙酸 | D.丙烯酸 |
与CH2=CH2®CH2Br—CH2Br的变化属于同一反应类型的是()
A.CH3CHO®C2H5OH B.C2H5Cl®CH2=CH2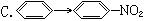 D.CH3COOH®CH3COOC2H5
D.CH3COOH®CH3COOC2H5
某醇与足量的金属钠反应,产生的氢气与醇的物质的量之比为1:1,则该醇可能是()
| A.甲醇 | B.乙醇 | C.乙二醇 | D.丙三醇 |
葡萄糖不能发生的反应有()
| A.酯化反应 | B.银镜反应 | C.还原反应 | D.水解反应 |