(每空2分,共16分)实验室欲用NaOH固体配制1.0 mol/L的NaOH溶液480 mL: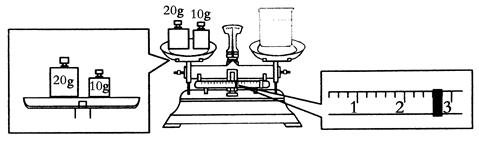
(1)配制时,必须使用的玻璃仪器有________、________、________、________。
(2)要完成本实验该同学应称出NaOH________g。
(3)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图,烧杯的实际质量为________g。
(4)使用容量瓶前必须进行的一步操作是________。
(5)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是________。
①没有洗涤烧杯和玻璃棒 ②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水 ④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
氢气是一种清洁能源,可以通过多种方法制得。
(1) 工业上用水煤气法制氢气,有关化学方程式是:
反应一:C( s) + H2O(g)
s) + H2O(g)  CO(g) + H2(g)△H> 0
CO(g) + H2(g)△H> 0
反应二:CO(g) + H2O(g)  CO2(g) + H2(g)△H < 0
CO2(g) + H2(g)△H < 0
①若反应一在t℃时达到化学平衡状态,则此温度下该反应的的平衡常数表达式
K = ;
②在427℃时将CO 和H2O(g)各0.01mol通入体积为2升的密闭容器中反应,5分钟时达到平衡状态,该反应的平衡常数是9,则CO的转化率是,用CO的浓度变化表示的反应率速v(CO)是mol /(L·min)。
(2)利用电解饱和食盐水也可制得氢气,下图为电解食盐水的示意图: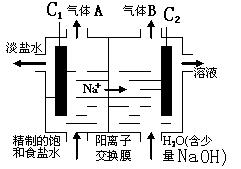
请回答:
① C1电极是极(填“阴”或“阳”),C2电极的电极反应式是。
②该电解反应的离子方程式是,
(3)通过下列方法也可以得到氢气。
已知: CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.2kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=-247.4 kJ·mol-1
1molCH4(g)与H2O(g)反应生成CO2(g)和H2(g)的反应热是kJ·mol-1。
2011年9月29日成功发射天宫一号的长征二号F型火箭巨大的推力来源于一个氧化还原反应,反应时偏二甲肼(C2H8N2)做燃料,N2O4做氧化剂,生成三种气体物质,完成并配平该燃烧反应的化学方程式:
C2H8N2 + N2O4=N2 ↑+ CO2↑ + ____
(1)火箭发射前低温加注的液态氧化剂N2O4是一种强酸性剧毒物质,常温下,纯净的N2O4是无色气体,可溶于水,且与水反应生成两种含氧酸,该反应的化
,
对上述反应中的各种物质,下列说法正确的是。
| A.N2O4只做氧化剂 | B.产物中两种酸都是强酸 |
| C.反应中水只做溶剂 | D.N2O4泄漏后可产生红棕色气体 |
(2)通过仪器分析燃烧剂偏二甲肼分子,得知其分子结构情况如下表:
符合上表结构及数据要求的同分异构体共有种,已知偏二甲肼的结构中有一个氮原子上没有连接氢原子,则偏二甲肼的结构简式是______。
铝、铁、碳元素的单质和化合物应用广泛。
(1)铝元素的原子结构示意图是____________,铁元素常见的化合价是。
(2)三种元素的单质及化合物均可以实现下列转化: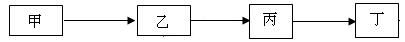
在上述每次转化时甲、乙、丙、丁四种物质中只有一种是单质,且四种物质中 均含有该种单质元素,请回答:
均含有该种单质元素,请回答:
①若丙是地壳中含量最多的金属元素的单质,丁易溶于水,溶液显碱性,则甲和乙是
和;丙到丁的离子方程式是。
②若乙是一种温室气体,相同条件下,丙和丁的溶液都显碱性,且丙的溶液的碱性强于丁的溶液的碱性,乙到丙的离子方程式是。
③若乙是有磁性的黑色晶体,在乙中加入稀硝酸后可得到丙,同时得到一种无色气体,该气体遇空气呈红棕色,该反应的化学方程式是;
将过量的甲加入丙的溶液中得到丁的溶液,然后在向其中滴入黄色铁氰化钾 (K3[Fe(CN)6])溶液后能发生复分解反应生成蓝色沉淀,该反应的化学方程式是
。
(3)钢铁在潮湿空气中容易被腐蚀,其中正极是(写名称),在潮湿的中性环境中的正极反应是,在下面方框中画一个牺牲阳极的阴极保护法装置,以防止钢铁被腐蚀。
醋酸是我们很熟悉的一种有机物。
(1)生活中可使用醋酸除暖瓶中的水垢,由此说明醋酸具有的性质是。
A.挥 发性 发性 |
B.酸性比碳酸强 | C.难电 离 离 |
D.易溶于水 |
(2)某同学为了解醋酸溶液的导电性进行了相应实验,右图为冰醋酸(无水醋酸晶体)在稀释过程中溶液的导电性变化关系图。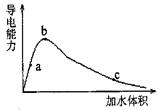
请回答:
①在稀释过程中,a 、b、c三处溶液的pH值由大到小的顺序是。
②从b点到c点,溶液中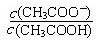 的比值(填“增大”、“减小”或“不变”)。
的比值(填“增大”、“减小”或“不变”)。
③ b点时溶液除水以外各种分子、离子的浓度由大到小的顺序是。
X 、Y、 Z、 W为四种常见的短周期元素。其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如下图所示:
| X |
Y |
|
| Z |
W |
请回答下列问题:
(1)W位于周期表中第______________周期,第___________族。
(2)X和氢可以构成+1价阳离子,其电子式是,Y的气态氢化物的稳定性
比Z的气态氢化物的稳定性(填“强”、或“弱”)。
(3)X的最高价氧化物的水化物与其氢化物能化合生成M, M的水溶液显酸性的原因是
_______________(用离子方程式表示)。
(4)①Y和Z可组成一种气态化合物Q,Q能与W的单质在潮湿环境中反应,反应的化学方程式是 。
。
②在一定条件下,化合物Q与Y的单质反应达平衡时有三种气态物质,反应时 ,每转移4mol电子放热190.0kJ,该反应的热化学方程式是。
,每转移4mol电子放热190.0kJ,该反应的热化学方程式是。