(18分)某校化学实验兴趣小组在“探究卤索单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入l~2滴溴水,振荡后溶液呈黄色。
提出问题 Fe3+、Br2谁的氧化性更强?
(1 )猜 想: ①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含 (填化学式,下同)所致。
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含 所致。
(2)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。
供选用的试剂:a.酚酞试液;b.CCl4;c.无水酒精;d.KSCN溶液。
请你在下表中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
| |
选用试剂 |
实验现象 |
| 方案1 |
|
|
| 方案2 |
|
|
(3)结论:氧化性:Br2>Fe3+。故在足量的稀氯化亚铁溶液中,加入l~2滴溴水,溶液呈黄色所发生的离子反应方程式为 。
(4)实验后的思考
①根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是:
(填离子的化学式)。
②在100 mL FeBr2溶液中通入2.24 L Cl2(标准状况),溶液中有1/2的Br-被氧气成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为 。
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
(1)A中反应的离子方程式为____________________。
(2)B中Sn极的电极反应式为____________________,
Sn极附近溶液的pH___________(填“增大”、“减小”或“不变”)。
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是____ ____________________。
____________________。
(1)下列反应中,属于放热反应的是,属于吸热反应的是。
①燃烧反应②炸药爆炸③酸碱中和反应④二氧化碳通过炽热的碳
⑤食物因氧化而腐败⑥Ba(OH)2·8H2O与NH4Cl反应⑦铁粉与稀盐酸反应
(2)写出(1)中⑥的化学方程式。
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖。在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同, 根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。
根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。
(1)下列物质中,其核磁共振氢谱中给出的峰值(信号)只有一个的是。
| A.CH3CH3 | B.CH3COOH | C.CH3COOCH3 | D.CH3OCH3 |
(2)化合物A和B的分子 式都是C2H4Br2, A的核磁共振氢谱图如下图所示,则A的结构简式为:,请预测B的核磁共振氢谱上有个峰(信号)。
式都是C2H4Br2, A的核磁共振氢谱图如下图所示,则A的结构简式为:,请预测B的核磁共振氢谱上有个峰(信号)。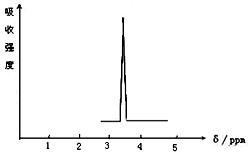
(3)化合物C的分子式是C10H14,核磁共振氢谱图如 下图所示,则C的结构简式为:。
下图所示,则C的结构简式为:。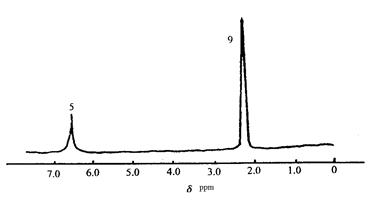
某烃A的相对分子质量是156,在CCl4溶液中跟Br2不起反应,但在光照下,Br2可以跟A起取代反应,取代产物的相对分子质量是235的有两种:产量较多的一种是B,产量较少的一种是C。另外,还可得到相对分子质量为314的产物多种。
(1)请写出A、B、C的结构简式:
ABC
(2)相 对分子质量为314的产物有种。
对分子质量为314的产物有种。
A、B、C、D是四种气态烃,其中A、B 、C能使溴水褪色。1摩尔C与2摩尔氯气完全加成,生成物分子中每个碳原子上都连有氢原子和氯原子。A与C、B与D分别具有相同的通式,A在催化剂存在下与氢气反应可得到B,在同温同压下B与氮气的密度相同,D没有同类的异构体,则四种气态烃的名称分别是:
、C能使溴水褪色。1摩尔C与2摩尔氯气完全加成,生成物分子中每个碳原子上都连有氢原子和氯原子。A与C、B与D分别具有相同的通式,A在催化剂存在下与氢气反应可得到B,在同温同压下B与氮气的密度相同,D没有同类的异构体,则四种气态烃的名称分别是:
A、B、C、D。