类比推理的方法在化学学习与研究中有广泛的应用,但有时会得出错误的结论。以下几个
类比推理结论中正确的是
| A.CO2通入Ba(NO3)2溶液中无沉淀生成,推出SO2通入Ba(NO3)2溶液中无沉淀生成 |
| B.在常温下,Na2CO3+2HCl=2NaCl+CO2↑+H2O,说明HCl酸性强于H2CO3; 在高温下,Na2CO3+SiO2= Na2SiO3+CO2↑,说明H2SiO3酸性强于H2CO3; |
| C.H2SO4为强酸,推出HClO4为强酸 |
| D.NH3的沸点高于PH3,推出CH4沸点高于SiH4 |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A.常温下,1 L 0.5 mol·L-1 NH4Cl溶液中含有3.01×1023个NH |
| B.1mol甲基(—CH3)所含的电子数为8NA |
| C.7.8g Na2O2与CO2完全反应,转移的电子数为0.1NA |
| D.80mL 10mol/L的浓盐酸与足量MnO2加热反应,转移的电子数为0.4NA |
下列有关实验过程中,一般不需要使用玻璃棒进行操作的是()
| A.蒸发 | B.过滤 | C.配制一定物质的量浓度的溶液 | D.制备氢氧化铁胶体 |
常温下,加水冲稀时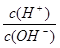 的值明显减小的溶液中,一定能大量共存的离子组是( )
的值明显减小的溶液中,一定能大量共存的离子组是( )
①K+、Cl-、NO、CH3COO- ②K+、Fe2+、I-、SO ③Ba2+、Cl-、NO、Na+
④Na+、Ca2+、Cl-、HCO ⑤K+、SO、Cl-、NO
| A.②③ | B.①③⑤ | C.②④ | D.②③⑤ |
从化学反应的分类角度来考虑下列反应原理,不属于同类的是()
| A.实验室制氯气 | B.实验室制备氨气 | C.实验室制氢气 | D.实验室制一氧化氮 |
化学与生活、社会密切相关。下列说法不正确的是( )
| A.从海带中提取碘单质的过程涉及氧化还原反应 |
| B.四川灾区重建使用了大量钢材,钢材是合金 |
| C.在食用盐中添加适量的碘酸钾预防大脖子病 |
| D.“钡餐”中使用的硫酸钡是弱电解质 |