等体积、等浓度的NaCl、MgCl2、AlCl3三种溶液分别与等物质的量浓度的AgNO3溶液恰好完全反应,则与NaCl、MgCl2、AlCl3三种溶液反应的AgNO3溶液的体积比为( )
| A.9:3:1 | B.1:2:3 | C.3:2:1 | D.6:3:2 |
根据表中信息判断,下列选项不正确的是
| 序号 |
反应物 |
产物 |
| ① |
KMnO4、H2O2、H2SO4 |
K2SO4、MnSO4… |
| ② |
Cl2、FeBr2 |
FeCl3、FeBr3 |
| ③ |
MnO4-… |
Cl2、Mn2+… |
A.第①组反应的其余产物为H2O和O2
B.第②组反应中Cl2与FeBr2的物质的量之比可能为1∶2
C.第③组反应中生成1 mol Cl2,转移电子2 mol
D.氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2
标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为c mol/L,则下列选项不正确的是
| A.ρ="(17V+22400" )/ (22.4+22.4V) |
| B.用水稀释该溶液,OH-的物质的量增加 |
| C.该溶液中共有6种微粒 |
| D.c="1000Vρ/(17V+22400)" |
将锌、铁、铜粉末按一定比例混合投入到一定量的硝酸中,微热,充分反应后过滤,弃去滤渣,滤液中金属阳离子情况不可能是
| A.只含Cu2+、Fe2+、Zn2+ | B.只含Zn2+ |
| C.只含Fe2+、Zn2+ | D.只含Cu2+、Fe3+、Zn2+ |
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是(已知:2NO2 N2O4△H<0)
N2O4△H<0)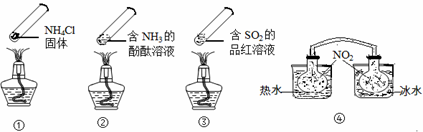
| A.加热时,①上部汇集了固体NH4Cl,说明NH4Cl的热稳定性比较好 |
| B.加热时,②、③溶液均变红,冷却后又都变为无色 |
| C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅 |
| D.四个“封管实验”中所发生的化学反应都是可逆反应 |
某课外活动小组的同学欲测定过氧化钠与碳酸钠混合物中过氧化钠的质量分数,他们先准确称量了a克样品,请你判断,在以下设计的各步后续实验方案中,不合理的是
| A.隔绝空气加热,冷却后,称量剩余固体质量为m 1 g |
| B.与足量稀盐酸反应并蒸干,称量剩余固体质量为m 2 g |
| C.与足量水反应并加热,收集到标准状况下V1 L干燥气体 |
| D.与足量稀硫酸反应并加热,收集到标准状况下V2 L 干燥气体 |