(12分) 氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素在元素周期表中的位置为 ;
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ;
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4(1) △H1= -19.5kJ·mol-1
②N2H4(1) + O2(g)= N2(g) + 2 H2O(g) △H2= -534.2kJ·mol-1
写出肼和N2O4反应的热化学方程式 ;
(4)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为
(5)下图是一个电化学过程示意图。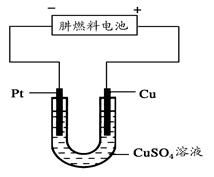
①写出铂片上发生的电极反应式____ ____。
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量变化128 g,则肼-空气燃料电池理论上消耗标准状况下的空气_____ ___L(假设空气中氧气体积含量为20%)。
(1)用盐酸检验牙膏中有无碳酸钙的反应的离子方程式是___ _①____,往苯酚溶液中加入几滴氯化铁溶液,观察到的现象是____②____。
_①____,往苯酚溶液中加入几滴氯化铁溶液,观察到的现象是____②____。
(2)将火柴燃烧生成的气体通入盛有少量高锰酸钾酸性溶液的试管中,可以观察到的现象是____③___,说明火柴燃 烧过程中有___④____气体(填名称或符号)生成,反应中高锰酸钾是____⑤____(填“氧化剂”、“还原剂”)
烧过程中有___④____气体(填名称或符号)生成,反应中高锰酸钾是____⑤____(填“氧化剂”、“还原剂”)
(3)往盐酸酸化的FeCl2溶液中,加入NaNO2溶液,除了气体之外还能够观察到的现象是___⑥____,反应的离子方程式____⑦___,反应中NaNO2是___⑧___(填“氧化剂”、“还原剂”)。
物质的分离是化学研究中常用的方法,填写下列物质分离时需使用的方法(不必叙述操作细节)。
(1)两种互不相溶的液体的分离①。
(2)固体和液体的分离②。
(3)含固体溶质的溶液中除去部分溶剂③。
(4)胶体中分离出可溶电解质④。
(5)几种沸点相差较大的互溶液体的分离⑤。
海水是一种丰富的资源,工业上从海水中可提取许多种物质,广泛应用于生活、生产、科技等方面。下图是某工厂对海水资源进行综合利用的示意图。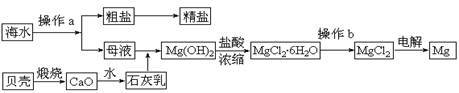
回答下列问题:
(1)流程图中操作a在蒸发结晶后进行(填操作名称)。
(2)工业上从海水中提取的NaCl,可用来制取纯缄,其简要过程如下:向饱和食盐水中
先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱。
①气体A、B是CO2或NH3,则气体A应是(填化学式)。
②滤液D中主要含有NH4Cl、NaHCO3等物质,工业上是向滤液D中通入NH3,并加入细小食盐颗粒,冷却析出不含有NaHCO3的副产品NH4Cl晶体,则通入NH3的作用是 。
(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是:
。
②操作b是在氛围中进行,若在空气中加热,则会生成Mg(OH)Cl。
(1)在T1℃时,向容积为2L的密闭容器甲中加入1molN2、3 molH2及少量固体催化剂,发生反应N2(g)+3H2(g) 2NH3(g)DH<0,10min时各物质的浓度不再变化,测得NH3物质的量为0.4mol。
2NH3(g)DH<0,10min时各物质的浓度不再变化,测得NH3物质的量为0.4mol。
①该反应在0~10min时间内H2的平均反应速率为mol·L-1·min-1,N2的转化率为。
②在T1℃时,若起始时在容器甲中加入0.5molN2、1.5 molH2、1molNH3,则达到平衡时NH3的物质的量为(填选项字母)
A.大于0.4mol B.等于0.4mol C.小于0.4mol
③下图是在T1℃时密闭容器甲中H2的体积分数随时间t的变化曲线,请在该图中补画出该反应在T2℃(T2>T1)时的H2体积分数随时间t的变化曲线。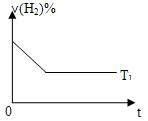
(2)明矾可做净水剂是因为(用离子方程式表示);
向明矾的水溶液中加入饱和的小苏打溶液发生反应的离子方程式为。
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时:正极的电极反应式是,负极的电极反应式是 。
(3)如图是一个电化学过程示意图。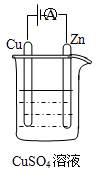
①锌片上发生的电极反应是 。
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化
128g,则肼一空气燃料电池理论上消耗标准状况下的空气L。
(假设空气中氧气体积含量为20%)