实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
①如图所示的仪器中,配制溶液肯定不需要的是__________________________ (填序号),配制上述溶液还需用到的玻璃仪器有 (填仪器名称)。
②配制0.1 mol/L NaOH溶液时,其正确的操作顺序是(字母表示,每个字母只能用一次) 。
| A.将容量瓶盖紧,振荡,摇匀 |
| B.改用胶头滴管加水,使溶液凹面恰好与刻度线相切 |
| C.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处 |
| D.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶 |
E.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
F.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
③配制0.1 mol/L NaOH溶液时,在实验中其他操作均正确,若定容时仰视容量瓶刻度线,则所配溶液浓度 0.1 mol/L(填“大于”、“等于”或“小于”)。
④配制0.5 mol/L硫酸溶液500 mL时,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为 mL(计算结果保留一位小数)。
⑤配制0.5 mol/L硫酸溶液时,在实验中其他操作均正确,若用量筒量取浓硫酸时仰视刻度线,则所配溶液浓度 0.5 mol/L(填“大于”、“等于”或“小于”)。
【原创】下表是元素周期表中的一部分,根据A—I在周期表中的位置,用元素符号或化学式回答下列问题:
| 周期族 |
IA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
Ⅷ |
| 1 |
A |
|||||||
| 2 |
B |
C |
L |
|||||
| 3 |
E |
F |
G |
D |
||||
| 4 |
H |
I |
(1)E和G形成的化合物的电子式______________,属于_____________化合物(“共价化合物”或者“离子化合物”)
(2)ABCEFGL中原子半径由大到小排列顺序___________________________(填写元素符号)
(3)ABCDEFGHIL中金属性最强_________非金属性最强__________化学性质最稳定的是________(填元素符号)
(4)F的单质与H的最高价氧化物的水化物反应的离子方程式________________________________
(5)ABEL形成的化合物________在生活中常被用来制作面包的发酵剂请写出相关化学反应方程式______________________________________________该化合物也能与E的最高价氧化物的水化物反应,请写出相关离子反应方程式______________________________________
没食子酸丙酯简称PG,结构简式为 ,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
(1)PG的分子式为 ,请写出PG分子中所含官能团的名称 ,1molPG与足量氢氧化钠溶液完全反应时,消耗的氢氧化钠的物质的量是 。
PG可发生如下转化:
(2)A的结构简式为 ,1mol没食子酸最多可与 mol H2加成。
(3)上图的有关变化中,属于氧化反应的有(填序号) 。
(4)从分子结构或性质上看,PG具有抗氧化作用的主要原因是(填序号) 。
| A.含有苯环 | B.含有羧基 | C.含有酚羟基 | D.微溶于食用油 |
(5)反应④的化学方程式为: 。
(6)B有多种同分异构体,写出其中符合下列要求的同分异构体的结构简式: 。
i.含有苯环,且苯环上的一溴代物只有一种;
ii.既能发生银镜反应,又能发生水解反应。
【原创】物质结构理论可以帮助人们理解物质变化的本质,进而研究反应规律和进行分子设计,请根据要求完成下列问题:
(1)金属具有延展性,而离子晶体容易破裂。试从结构的角度分析其中的主要原因____________;
(2)第三周期基态原子有2个未成对电子且电负性最大的元素是_____;
(3)水可以电离H3O+,下列分子中,中心原子的杂化方式与H3O+中氧原子的杂化方式相同的是_____
a.NO2-中的氮原子 b.ClO3-中的氯原子
c.NH2-中的氮原子 d.CH2=CH2中的碳原子
(4)F、Mg、K三种元素形成的晶体晶胞结构如图所示,写出其化学式________。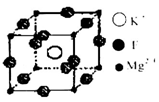
新近出版的《前沿科学》杂志刊发的中国环境科学研究院研究员的论文《汽车尾气污染及其危害》,其中系统地阐述了汽车尾气排放对大气环境及人体健康造成的严重危害。目前降低尾气的可行方法是在汽车排气管上安装催化转化器。NO和X气体均为汽车尾气的成分,这两种气体在催化转换器中发生反应:① 2X(g)+2NO(g) N2(g)+2CO2(g) △H=-a kJ·mol-1。
N2(g)+2CO2(g) △H=-a kJ·mol-1。
(1)上述信息中气体X的化学式为 。
(2)已知② 2NO(g)+O2(g)=2NO2(g) △H=-b kJ·mol-1;X的燃烧热△H=-c kJ·mol-1。书写在消除汽车尾气中NO2的污染时,NO2与X的可逆反应的热化学反应方程式 。
(3)在一定温度下,将1.0mol NO、1.2mol气体X通入到固定容积为2L的容器中,反应过程中部分物质的浓度变化如图所示: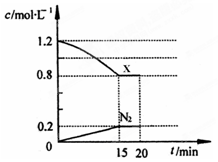
①有害气体NO的转化率为 ,0~15min NO的平均速率v(NO)= 。
②20min时,若改变反应条件,导致X浓度增大,则改变的条件可能是 (选填序号)。
| A.缩小容器体积 | B.增加CO2的量 |
| C.升高温度 | D.加入催化剂 |
③若保持反应体系的温度不变,20min时再向容器中充入NO、N2各0.4mol,化学平衡将 移动(选填“向左”、“向右”或“不”)。
(14分)I.下表为元素周期表的一部分:(用元素符号或化学式填空)
| 族 周期 |
||||||||
| ① |
||||||||
| ② |
||||||||
| ③ |
④ |
⑤ |
⑥ |
|||||
(1)写出元素④在周期表中的位置______________。
(2)②、③、⑤的原子半径由大到小的顺序为_________________________。
(3)④、⑤、⑥的气态氢化物的稳定性由强到弱的顺序是_________________________。
(4)①、②、③、⑥中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
II.由上述部分元素组成的物质间,在一定条件下,可以发生下图所示的变化,其中A是一种淡黄色固体。请回答: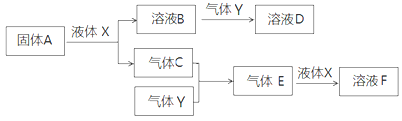
(1)写出固体A与液体X反应的离子方程式 。
(2)气体Y是一种大气污染物,直接排放会形成酸雨。可用溶液B吸收,当B与Y物质的量之比为1:1且恰好完全反应时,所得溶液D的溶质为 (填化学式)。
(3)写出气体C与气体Y反应的化学方程式 。