下列实验方案设计中,可行的是 ( )
| A.加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉 |
| B.用萃取的方法分离汽油和煤油 |
| C.用溶解、过滤的方法分离KNO3和NaCl固体的混合物 |
| D.将H2和O2的混合气体通过灼热的氧化铜,以除去其中的H2 |
下列各组元素的性质递变情况错误的是()
| A.Li、Be、B原子最外层电子数依次增多 | B.P、S、Cl元素最高正价依次升高 |
| C.N、O、F原子半径依次增大 | D.Na、K、Rb的金属性依次增强 |
碱金属元素都是典型的活泼金属,其原因是()
| A.密度小,熔、沸点低 | B.在自然界中无游离态存在 |
| C.常温下易液化 | D.最外层只有一个电子,容易失去 |
决定化学反应速率的主要因素是()
| A.参加反应的物质本身的性质 | B.催化剂 |
| C.温度、压强以及反应物的接触面 | D.反应物的浓度 |
在元素周期表中金属元素与非金属元素分界线附近的元素能用于制造()
| A.合金 | B.半导体 | C.催化剂 | D.农药 |
下列各组物质中,互为同位素的是()
| A.T2O与D2O | B.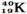 与 与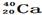 |
| C.O2和O3 | D.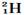 和 和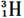 |