(1)在常温下,0.5mol甲醇在氧气中完全燃烧生成CO2和液态水,放出热量363.3kJ.写出该反应的热化学方程式: _________________________
(2)请设计一个燃料电池:电解质为强碱溶液,Pt作电极,在电极上分别通入甲醇和氧气。通入甲醇的电极应为 极(填“正”或“负”),该电极上发生的电极反应式为 。
(3)用Pt电极电解盛有1L pH=6的硝酸银溶液,如图甲所示,则右边电极上发生的电极反应式为 .
(4)某化学学习兴趣小组为了研究金属的腐蚀现象,将一枚铁钉放在“84”消毒液(NaClO)中,某同学设计了如图乙所示实验装置,写出石墨极上发生的电极反应式:
在2L密闭容器中,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
⑴写出该反应的平衡常数表达式:K=__________________________
已知:K(300℃)>K(350℃),该反应是________热反应。
⑵右图中表示NO2的变化的曲线是____________。用O2表示从0~2s内该反应的平均速率v=__________________
⑶能说明该反应已经达到平衡状态的是___________
a、v(NO2)=2v(O2) b、容器内压强保持不变
c、v逆(NO)=2v正(O2) d、容器内的密度保持不变
⑷为使该反应的反应速率增大,且平衡向正反应方向移动的是__________
a、及时分离出NO2气体 b、适当升高温度
c、增大O2的浓度 d、选择高效的催化剂
实验室需要0.1 mol·L-1NaOH溶液450 moL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
⑴如图所示的仪器中配制溶液肯定不需要的是(填序号);配制上述溶液还需用到的玻璃仪器是(填仪器名称)。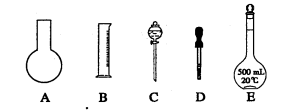
⑵下列操作中,容量瓶所不具备的功能有(填序号)。
| A.配制一定体积准确浓度的标准溶液 |
| B.贮存溶液 |
| C.测量容量瓶规格以下的任意体积的液体 |
| D.准确稀释某一浓度的溶液 |
E.用来加热溶解固体溶质
⑶请计算需用托盘天平称取固体NaOH的质量为g。某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,烧杯的实际质量为g。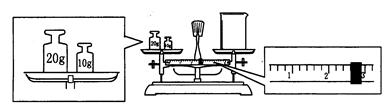
⑷根据以上计算得知,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为mL(计算结果保留一位小数)。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是。
设水的电离平衡曲线如图所示: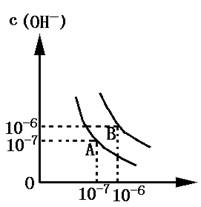
⑴若以A点表示水在电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态到B点,则此时水的离子积从增加到.
⑵将pH=8的Ba(OH)2溶液与PH=5的稀盐酸相混合,并保持100℃的恒温,欲使混合溶液的pH=7,则Ba(OH)2与盐酸的体积比为
同素异形体相互转化的反应热相当少而且转化速率较慢,有时还很不完全,测定反应热很困难,现在可根据盖斯定律进行计算。
已知:P4(固体.白磷)+5O2(气体)= P4O10(固体) △H=-2983.2kJ·mol-1 ①
P(固体.红磷)+O2(气体)=P4O10(固体) △H=-738.5kJ·mol-1 ②
⑴由热化学方程式来看,更稳定的磷的同素异形体是
⑵试写出白磷转化为红磷的热化学方程式
(共4分) A、B、C、D都是中学化学常见的物质,其中A、B、C均含同一种元素。在一定条件下相互转化关系如下图所示(部分产物已略去)。请按要求回答下列问题: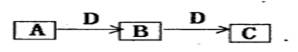
⑴若B、C为氧化物,B转化为C时,质量增加25%,C能够与水反应生成一种强酸,则B转化为C的化学方程式是:
⑵若D为某金属单质,向C的溶液中滴加硝酸银溶液,产生不溶于稀硝酸的白色沉淀,则B的化学式是