有人曾建议用AG表示溶液的酸度,AG的定义为:AG=lg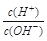 ,室温下实验室用0.01 mol·L-1的氢氧化钠溶液滴定20 mL相同浓度的醋酸溶液,滴定曲线如右图所示。下列有关叙述正确的是( )
,室温下实验室用0.01 mol·L-1的氢氧化钠溶液滴定20 mL相同浓度的醋酸溶液,滴定曲线如右图所示。下列有关叙述正确的是( )
| A.A点时加入氢氧化钠溶液体积为20 mL |
| B.室温时0.01 mol·L-1的醋酸溶液pH=4 |
| C.OA段溶液中:c(CH3COO-)> c(CH3COOH) |
| D.若B点时加入NaOH溶液40 mL,所得溶液中:c(CH3COO-)+2 c(CH3COOH) = c(OH-) - c(H+) |
下列叙述错误的是
| A.乙烯和苯都能使溴水褪色,褪色的原因相同 |
| B.淀粉、油脂、蛋白质都能水解,但水解产物不同 |
| C.煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
| D.乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中少量乙酸可用饱和Na2CO3溶液除去 |
下列各原子或原子团,不属于官能团的是
| A.—CH3 | B.—Br | C.—NO2 | D.>C=C< |
下列反应达到化学平衡后,加压或降温都能使化学平衡向逆反应方向移动的是
A.SO2(g)+NO2(g)  SO3(g)+NO(g)△H<0 SO3(g)+NO(g)△H<0 |
B.C(s)+CO2(g)  2CO(g)△H>0 2CO(g)△H>0 |
C.4NH3(g)+5O2(g)  4NO(g)+6H2O(g)△H<0 4NO(g)+6H2O(g)△H<0 |
D.H2S(g)  H2(g)+S(s)△H>0 H2(g)+S(s)△H>0 |
以下是几种常见的实验室制取气体的装置,其中可用于制取乙炔的是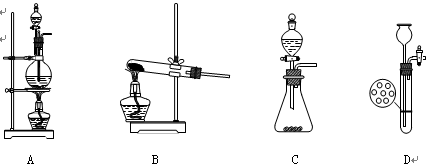
胡锦涛同志在十七大报告中指出,应加强能源资源节约和生态环境保护,增强可持续发展能力。下列行为与之不相符的是
| A.大量使用化学肥料,提高农作物的产量和质量 |
| B.将作物秸秆通过化学反应转化为乙醇用作汽车燃料 |
| C.使用资源节约型、环境友好型的生物降解塑料包装 |
| D.推广煤炭脱硫技术、减少直接燃煤,防止酸雨发生 |