某同学将某种金属分别与等体积的甲、乙两种溶液反应,所加金属的质量与相同条件下产生气体的体积关系如图所示,下列推论可能正确的是( )
| A.金属是镁,甲溶液为0.2 mol/L盐酸,乙溶液为0.1 mol/L盐酸 |
| B.金属是铁,甲溶液为pH=1的醋酸溶液,乙溶液为pH=1的盐酸 |
| C.金属是铝,甲溶液为0.1 mol/L盐酸,乙溶液为0.1 mol/L氢氧化钠溶液 |
| D.金属是铝,甲溶液为0.1mol/L氢氧化钠溶液,乙溶液为0.1 mol/L盐酸 |
下列反应的离子方程式正确的是
A.HCO3-的水解方程式为:HCO3-+H2O H2CO3+OH— H2CO3+OH— |
| B.氢氧燃料电池的负极反应式:O2 + 2H2O+ 4e-=4OH- |
C.用铜做电极电解NaCl溶液:2Cl-+2H2O Cl2↑+H2↑+2OH— Cl2↑+H2↑+2OH— |
D.用惰性电极电解CuCl2溶液:2Cu2++2H2O 4H++O2↑+2Cu 4H++O2↑+2Cu |
下列说法正确的是
| A.铅蓄电池放电时的负极和充电时的阳极均发生还原反应 |
| B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
C.N2(g)+3H2(g) 2NH3(g) △H<0,其他条件不变时升高温度,反应速率v(H2)和氢气的平衡转化率均增大 2NH3(g) △H<0,其他条件不变时升高温度,反应速率v(H2)和氢气的平衡转化率均增大 |
| D.纯碱溶于热水中去污效果增强,说明纯碱的水解是放热反应 |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.1 L 0.1mol·L-1的氨水含有0.1NA个OH- |
| B.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA |
| C.在电解精炼粗铜的过程中,当阴极析出32 g铜时转移电子数为NA |
| D.25℃时,pH =13的Ba(OH)2溶液中含有OH-的数目为0 .1 NA |
常温下,下列溶液中各组离子一定能大量共存的是
| A.使甲基橙呈红色的溶液中:Na+、AlO2-、NO3-、CO32- |
| B.由水电离产生的c(H+)=10-12mol·L-1的溶液:NH4+、SO42-、HCO3-、Cl- |
| C.c(H+)/c(OH-)= 1×1014的溶液: Ca2+、Na+、ClO-、NO3- |
D.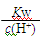 =0.1 mol·L-1的溶液:Na+、K+、CO32-、NO3- =0.1 mol·L-1的溶液:Na+、K+、CO32-、NO3- |
下列物质的系统命名中,错误的是
A.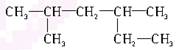 2,4-二甲基己烷 2,4-二甲基己烷 |
B.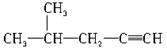 2-甲基-4-戊炔 2-甲基-4-戊炔 |
C.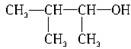 3-甲基-2-丁醇 3-甲基-2-丁醇 |
| D.CH3—CHBr—CHBr—CH3 2,3-二溴丁烷 |