甲、乙、丙、丁四种物质之间存在如图所示转化关系,且甲、乙、丙均含有相同的某种元素。下列推断错误的是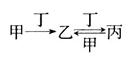
| A.若丙为CO2,则甲可以是焦炭 |
| B.若丁为O2,则甲可以是N2 |
| C.若丁为Fe,则甲可以是Cl2 |
| D.若丁为CO2,则甲可以是NaOH溶液 |
有人认为CH2=CH2与Br2的加成反应,实质是Br2先断裂为Br+和Br-,然后Br+首先与CH2=CH2一端碳原子结合,第二步才是Br-与另一端碳原子结合。根据该观点如果让CH2=CH2与Br2在盛有NaCl和NaI的水溶液中反应,则得到的有机物不可能是
| A.BrCH2CH2Br | B.ClCH2CH2Cl | C.BrCH2CH2I | D.BrCH2CH2Cl |
绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中,下列过程不符合这一思想的是
A.氢气、CO合成甲醇: 2H2+CO CH3OH CH3OH |
B.烯烃与水煤气发生反应:RCH=CH2+CO+H2 RCH2CH2CHO RCH2CH2CHO |
| C.CH4与Cl2反应制取CCl4 |
| D.氯乙烯合成聚氯乙烯 |
膳食纤维具有突出的保健功能,是人体的“第七营养素”。木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示。下列有关芥子醇的说法正确的是
| A.芥子醇的分子式是C11H14O4,属于芳香烃 |
| B.芥子醇分子中所有碳原子不可能在同一平面 |
| C.芥子醇能与3mol溴水反应 |
| D.芥子醇能发生的反应类型有氧化、取代、加成 |
杀虫剂“阿乐丹”的结构如图,关于该有机物的说法,正确的是
| A.可溶于水 | B.能发生银镜反应 |
| C.能与溴水反应 | D.不能水解 |
下列物质属于油脂的是
④润滑油 ⑤花生油 ⑥石蜡
| A.①⑤ | B.④⑤ | C.①② | D.①③ |