对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
| A.达到化学平衡时4v正(O2)=5v逆(NO) |
| B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
| C.达到化学平衡时,若增大容器容积,则正反应速率减小,逆反应速率增大 |
| D.化学反应速率关系:2v正(NH3)=3v正(H2O) |
接触法制硫酸的生产过程中,下列措施能提高硫酸的产率的是()
| A.控制接触室内的温度在450℃左右 |
| B.沸腾炉中通入过量空气 |
| C.对炉气进行除尘、洗涤、干燥处理 |
| D.接触室中用V2O5作催化剂 |
在下列气体的制取中,均用到浓硫酸。浓硫酸只起脱水剂作用的是()
| A.浓硫酸与甲酸加热制取CO |
| B.浓硫酸与铜反应制取SO2 |
| C.浓硫酸与无水乙醇反应制取乙烯 |
| D.浓硫酸与亚硫酸钠反应制取SO2 |
在硫酸工业制法中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器的接触室(见下图)。按此密闭体系中气体的流向,则在A处流出的气体为()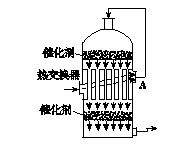
| A.SO2 | B.SO3O2 | C.SO2O2 | D.SO2SO3 |
下列关于三氧化硫的叙述正确的是()
| A.标准状况下三氧化硫是一种无色气体 |
| B.三氧化硫与水反应放出大量的热 |
| C.接触法制硫酸中常用水吸收三氧化硫 |
| D.三氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水 |
在硫酸的工业制法中,下列对生产操作与生产操作的主要原因的说明都正确的是()
| A.硫铁矿燃烧前需要粉碎,因为大块的硫铁矿不能燃烧 |
| B.从沸腾炉出来的炉气需要净化,因为炉气中SO2会与杂质反应 |
| C.SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率 |
| D.用98.3%的浓硫酸吸收,目的是防止形成酸雾,以便使SO3吸收完全 |