(1).将质量比为14 :15的N2和NO混合,则混合气体中N2和NO的物质的量之比为______,氮原子和氧原子的个数比为________。
(2).同温同压下,质量相同的五种气体: ① CO2 ② H2 ③ O2 ④ CH4 ⑤ SO2
所占的体积由大到小的顺序是(填序号,下同)_________________;
密度由大到小的顺序是_________________________________。
(3).VmL Al2(SO4)3溶液中含Al3+ ag,取V/4mL溶液稀释到VmL,则稀释后溶液中的SO42-的物质的量浓度是(单位为mol/L)______________。
(4).有一质量为mg,相对分子质量为M的某种强碱M (OH)2,在一定温度下,完全溶解在水中得到VmL饱和溶液,若此溶液的密度为ρg/cm3,则该溶液中OH-的物质的量浓度为________,溶质的质量分数为________。
有四种无色液体:60%的酒精、福尔马林、甲酸和醋酸。只使用一种试剂M鉴别它们,其鉴别过程如下: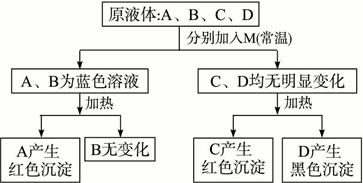
(1)试填写A—D所含有机物的结构简式。
A:______________,B:_______________,C:_______________,D:______________。
(2)试剂M的化学式:______________________________。
A是光合作用生成糖类的中间体,是糖类在动物体内代谢的中间产物,各物质间的反应关系如下: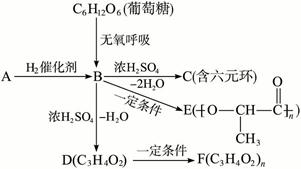
已知:①A的分子式为C3H4O3,可与乙醇生成有香味的物质。
②将A与Cu(OH)2悬浊液加热反应无红色沉淀生成。
③E与F均为高分子化合物。
④葡萄糖无氧呼吸的中间产物可以是乙醇或乳酸,而此题中的B是酸奶的主要成分。
根据以上信息,完成下列问题。
(1)写出下列物质的结构简式:
A. _________________,B. _________________,F. _________________。
(2)写出下列反应方程式:
D→F:_________________,B→C:_________________,B→E:_________________。
(3)A有多种同分异构体,请写出其中的任意两种:______________、_______________。
在安徽省阜阳市,由于被喂食几乎完全没有营养的劣质奶粉,13名可爱的小天使夭折,近200名婴儿患上严重营养不良症。据调查劣质奶粉主要是以各种廉价的食品原料如淀粉、蔗糖等全部或部分替代乳粉,再用奶香精等进行调香调味制成,没有添加婴儿生长发育所必需的维生素和矿物质。用这样的奶粉喂养婴儿,将会严重影响婴儿的生长发育。
(1)婴幼儿配方粉及婴幼儿补充谷粉通用技术条件规定:①0—6个月婴儿食用的婴儿配方粉:蛋白质含量10.0%—20.0%,脂肪含量≥20.0%;②婴幼儿补充谷粉(4个月龄以上婴幼儿的补充食品——非主食品):蛋白质含量≥5.0%;③较大婴儿和幼儿(6—36个月)食用的配方粉:蛋白质含量5%—25%;脂肪含量15.0%—25.0%。据以上技术标准判断劣质奶粉主要是_________________成分不达标及缺乏所必需的维生素和矿物质。
(2)脂肪、淀粉、蛋白质是三种重要的营养成分,其中_________________不是高分子化合物,它们都在人体内能发生_________________反应,脂肪的产物是_________________,淀粉的最终产物是_________________,蛋白质的最终产物是_________________。
(3)据调查“杀人奶粉”中含有增添乳香风味的“奶精”。奶精的配方主要是玉米糖浆和部分氢化的植物油。奶精的色泽来自食用色素,牛奶的风味来自人工香料。已知该人工香料中含香树脂醇,香树脂醇为三萜醇,结构中含有六个异戊二烯单位。判断香树脂醇肯定具有的性质()
①加成 ②加聚 ③溶液显酸性 ④可与Na2CO3溶液反应 ⑤与金属钠反应
| A.①②③ | B.①②⑤ |
| C.②③⑤ | D.①②⑥ |
将肥皂液分装在两支试管中,向第一支试管中加入稀硫酸,有____________产生,向第二支试管中加入MgCl2溶液,则产生____________,有关反应的离子方程式为:_____________________________________,_____________________________________。
下图为相互串联的甲、乙两电解池,试回答:
(1)若甲池利用电解原理在铁上镀银,则A是_____________、_____________(填电极材料和电极名称),电极反应是__________________________;B(要求同A)是______________、___________,电极反应式是_____________________________________________,应选用的电解质溶液是_____________。
(2)乙池中若滴入少量酚酞试液,开始电解一段时间,铁极附近呈_____________色,C极附近呈_____________色。
(3)若甲槽阴极增重43.2g,则乙槽中阳极上放出的气体在标况下的体积_____________mL。
(4)若乙槽中剩余溶液仍为400mL,则电解后所得溶液的物质的量浓度为_____________mol·L-1,pH等于_____________。