已知:pAg=-lg{c(Ag+)},KspAgCl=1×10-12如图是向10mLAgNO3溶液中逐渐加入0.1 mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线)。根据图象所得下列结论正确的是( )
(提示:KspAgCl>KspAgI)
| A.原AgNO3溶液的物质的量浓度为0.1 mol·L-1 |
| B.图中x点的坐标为(10,6 ) |
| C.图中x点表示溶液中Ag+与Cl— 浓度相同 |
| D.把0.1 mol·L-1的NaCl换成0.1 mol·L-1NaI则图象在终点后变为虚线部分 |
下列各项所述的两个量,前者一定大于后者的是
 ①纯水在25℃和80℃的pH
①纯水在25℃和80℃的pH ②1mol NaHSO4和1molNa2SO4在熔化状态下的离子数
②1mol NaHSO4和1molNa2SO4在熔化状态下的离子数 ③25℃时,等体积且pH都等于3的盐酸和AlCl3的溶液中,已电离的水分子数
③25℃时,等体积且pH都等于3的盐酸和AlCl3的溶液中,已电离的水分子数 ④Na+和F-的离子半径
④Na+和F-的离子半径
| A.②④ | B.只有① | C.①③ | D.只有② |
设NA为阿伏加德罗常数,下列说法正确的是
| A.标准状况下,5.6 L四氯化碳含有的分子数为0.25NA |
| B.1 mol C10H22分子中共价键总数为30NA |
| C.58.5g氯化钠可以构成NA个氯化钠晶胞 |
| D.标准状况下,22.4 L任意比的氢气和氯气的混合气体中含有的分子总数均为NA |
普通水泥在固化过程中自由水分子减少并产生胶体,溶液呈碱性。根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间。此法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的是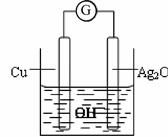
| A.水泥是一种新型无机非金属材料 |
| B.测量原理示意图中,Ag2O为负极 |
| C.负极的电极反应式为:2Cu+2OH—-2e—=Cu2O+H2O |
| D.电池工作时,OH-向正极移动 |
生活中常用到一些化学知识,下列分析中正确的是
| A.医疗上可用硫酸钡作x射线透视肠胃的内服药,是因为硫酸钡既不溶于水又不溶于酸 |
| B.某雨水样品放置一段时间后pH由4.68变为4.00,是因为水中溶解的CO2增多 |
| C.蛋白质加入饱和硫酸钠溶液会发生变性 |
| D.加碘食盐中添加碘酸钾而不用碘化钾,是因为碘酸钾能溶于水而碘化钾不溶于水 |
下列说法不正确的是
A.相同条件下,溶液中 、 、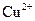 、 、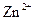 的氧化性依次减弱 的氧化性依次减弱 |
| B.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
| C.对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同 |
D.根据反应2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g)需在300℃进行可推测该反应是吸热反应 CH3CH2OH(g)+3H2O(g)需在300℃进行可推测该反应是吸热反应 |