下列物质中,导电性能最差的是()
| A.熔融的氢氧化钠 | B.石墨棒 | C.盐酸溶液 | D.固态氯化钾 |
室温下,在强酸性和强碱性溶液中都不能大量共存的离子组是( )
| A.NH4+、Cu2+、Cl-、NO3- |
| B.K+、Na+、SO32-、S2- |
| C.K+、Na+、AlO2-、SO42- |
| D.Ba2+、Fe2+、NO3-、Br- |
下列离子方程式正确的是( )
A.碳酸钙和盐酸反应:CO32-+2H+ H2O+CO2↑ H2O+CO2↑ |
B.向氢氧化钡溶液中加硫酸溶液:Ba2++SO42- BaSO4↓ BaSO4↓ |
C.向稀盐酸溶液中加铁:3Fe+6H+ 3Fe3++3H2↓ 3Fe3++3H2↓ |
D.向硝酸银溶液中加盐酸:Ag++Cl- AgCl↓ AgCl↓ |
无论在酸性还是碱性溶液中,都能大量共存的离子组是()
①K+、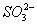 、S2-、
、S2-、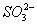 ②Na+、Cu2+、
②Na+、Cu2+、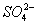 、Cl-③Br-、Ba2+、Cl-、K+④Ca2+、K+、
、Cl-③Br-、Ba2+、Cl-、K+④Ca2+、K+、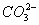 、
、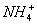 ⑤Cl-、Na+、
⑤Cl-、Na+、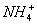 、
、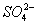 ⑥Mg2+、
⑥Mg2+、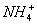 、
、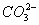 、F-
、F-
| A.①② | B.①④ | C.③⑤ | D.②⑥ |
某100 mL溶液中含H2SO40.50 mol,加入下列物质,溶液导电性增强的是()
| A.0.50molBa(OH)2 | B.100mL水 |
| C.0.50mol酒精 | D.0.50molNa2SO4 |