(每个方程式2分,其余每空1分,共8分)现有下列物质:①KI ②铜 ③稀硝酸 ④NH3 ⑤NaHSO4 ⑥Ba(OH)2 ⑦氢氧化铁胶体 ⑧氨水
(1)按物质的分类方法填写表格的空白处(填物质编号)
| 分类标准 |
电解质 |
盐 |
非电解质 |
混合物 |
| 属于该类的物质 |
|
|
|
|
(2)上述某两种物质在溶液中可发生离子反应:H++OH-=H2O,写出该离子反应对应的化学方程式 。
(3)物质①的稀溶液在空气中被氧化,加入淀粉溶液显蓝色,则反应的离子方程式为 。
X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y的最高正价与最低负价的代数和为2,Z与X原子最处层电子数相同。回答下列问题:
(1)X、Y和Z的元素符号分别为、、_。
(2)选用以上元素组成一种离子化合物,该化合物为______。
(3)X和Y组成的化合物Q中,既含有极性共价键又含有非极性共价键,Q的分子式是。Q在空气中点燃时,迅速而安全的燃烧,其反应产物没有任何污染,燃烧时的化学方程式为;Q还可将酸性工业废水中的Cr2O72-还原为Cr3+,氧化产物为常见气体。相应的离子方程式为。
氯、溴、碘、钠、镁、锰、锂、铀等元素在海洋中被富集。海洋开发利用和维权是国家战略。
(1)以上元素在海水中的存在形态是___________(选填①游离态②化合态③不确定)
(2)以下变化属于化学变化的是__________________________:
① 发生核裂变,②重氢(2H)发生核聚变,③LiH做野外生氢剂,④海水晒盐
发生核裂变,②重氢(2H)发生核聚变,③LiH做野外生氢剂,④海水晒盐
(3)由氯气和晒盐后的卤水制取液溴的离子方程式______________________________;由石灰乳和卤水沉淀出镁元素的离子方程式_____________________________________;由海带灰可浸出KI,由某种矿盐可浸出KIO3,二者在盐酸中反应可生成碘单质,反应的离子方程式__________________________________。
(4)工业由氯化钠制取金属钠的化学方程式为____________________________;工业制镁采用电解熔融氯化镁,不采用电解熔融氧化镁的原因是_______________________
(5)海底富集多种矿物结核,锰结核是其中的一种。锰结核中主要含有MnO2和Fe2O3。一种质量比约为m(Mn):m(Fe)=55:448的合金钢(其它元素略),具有抗御激烈冲击和磨损的能力,可做航母甲板等。欲通过铝热反应炼得这样的合金,MnO2、Fe2O3、Al的投料比(按物质的量之比)约为_______________。
硫及其化合物在自然界普遍存在、容易转化。
Ⅰ.火山喷发、生物质降解时产生的有毒气体H2S、SO2等进入大气后,因一些自然转化而得以消除。如
(1)H2S和SO2分子碰撞时,污染会降低。反应方程式为_________________________。
(2)H2S在常温下,会被空气逐渐氧化,反应方程式为_________________________。
(3)SO2在飘尘催化下,会被空气氧化为SO3,遇水生成硫酸,硫酸遇石灰岩转化为稳定的石膏矿物(CaSO4·2H2O)。SO2被氧化的化学方程式为_____________________________。
在环保措施上,这会给我们带来“师法自然”的启示。
Ⅱ.人为过度排放二氧化硫等,会超出自然净化吸收能力,带来严重环境污染。“石灰-石膏法”和“烧碱法”是工业上常用的工业烟气脱硫法。
(4)“石灰-石膏法”吸收二氧化硫的流程为:
由SO2等生成石膏的总化学方程式为________________________________________。
(5)“烧碱法”是用氢氧化钠浓溶液吸收含二氧化硫的烟气,其优点是氢氧化钠碱性强、吸收快、效率高。化学方程式为______________________________________。但烧碱的价格较贵(石灰0.36元/kg,烧碱2.90元/kg)。
(6)若将“石灰-石膏法” 和“烧碱法”结合起来对烟气脱硫,则会产生快速高效低成本无污染的好效果,最终仍得到石膏产品。请在下列流程图的①~④处填写物质的化学式: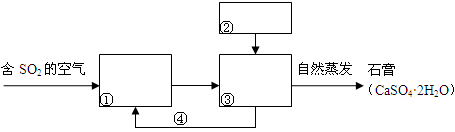
在学习了铜元素的性质之后,小明同学做了H2O2与铜的有关探究实验:
实验一:将铜丝置于装有H2O2溶液的试管中,没有气体产生;加热溶液时,观察到铜丝表面产生大量气体。
实验二:将铜丝置于装有硫酸酸化的H2O2溶液的试管中,溶液迅速变蓝。同时产生大量气体。
请回答下列问题:
(1)上述实验一(加热时)、实验二中铜丝表面均产生了大量气体,该气体是。
(2)写出在酸性条件下H2O2氧化铜丝的离子方程式:。
(3)H2O2能发生多种化学反应,等物质的量的H2O2在仅作氧化剂的反应、仅作还原剂的反应和分解反应中转移的电子数目之比为。
小明同学设计了以废铜屑制取硫酸铜的三个方案:
①认为最佳方案是。
②简述另两个方案的不足之处:。
高锰酸钾是一种重要的化工产品。如图是工业上用软锰矿制备高锰酸钾的一种工艺流程。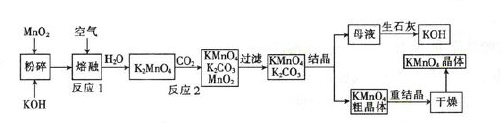
(1)KMnO4稀溶液是一种常用的消毒剂,其消毒机理与(填字母)相似。
| A.75%酒精 | B.O3 | C.二氧化硫 | D.漂白粉 |
(2)写出上述流程中反应2的化学方程式:__
(3)上述流程中可以循环使用的物质有CO2、和。(填化学式)
(4)若不考虑制备过程中的损失和整套装置的物质循环,则1 molMnO2可制得___gKMnO4。