经氯气消毒的自来水,若用于配制以下溶液:①NaOH ②AgNO3 ③Na2CO3 ④FeSO4 ⑤ KI ⑥Na2S ⑦Na2SO3,会使配制的溶液变质的是
| A.全部 | B.②④⑤⑥⑦ | C.①②⑤ | D.④⑥ |
下列事实可以用勒夏特列原理解释的是
| A.新制的氯水在光照条件下颜色変浅 |
| B.使用催化剂,提高合成氨的产率 |
| C.高锰酸钾(KMnO4)溶液加水稀释后颜色変浅 |
| D.H2、I2、HI平衡混合气体加压后颜色变深 |
在密闭容器中进行如下反应:A(s)+2B(g) 3C(g)△H<0,达平衡后,改变下列反应条件,相关叙述正确的是
3C(g)△H<0,达平衡后,改变下列反应条件,相关叙述正确的是
| A.加入少量A,正反应速率增大,平衡向正反应方向移动 |
| B.降低温度,正反应速率加大,逆反应速率变小,平衡向正反应方向移动 |
| C.增大压强,正反应速率和逆反应速率都增大,平衡向逆反应方向移动 |
| D.增大压强,能加快反应速率的主要原因是增大了活化分子的百分数 |
在钢铁腐蚀过程中,下列六种变化可能发生的是
①O2被还原 ②产生H2 ③Fe(OH)3失水形成Fe2O3·xH2O④杂质碳被氧化
⑤镀层破损后,镀锌铁板比镀锡铁板更耐腐蚀
| A.只①② | B.只②③④ | C.①②③⑤ | D.①②③④⑤ |
恒温恒容的情况下,反应A2(g)+B2(g) 2AB(g)达到平衡状态的标志是
2AB(g)达到平衡状态的标志是
| A.容器内气体的密度不随时间而变化 |
| B.容器内的总压强不随时间而变化 |
| C.单位时间内生成2n mol AB的同时,生成n mol的B2 |
| D.A2、B2、AB的反应速率比为2:2:1的状态 |
某温度时,N2+3H2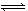 2NH3的平衡常数K="a," 则此温度下,NH3
2NH3的平衡常数K="a," 则此温度下,NH3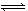 3/2H2+1/2N2的平衡常数为
3/2H2+1/2N2的平衡常数为
A.aˉ1/2 B.a1/2 C.1/2a D.aˉ2