X、Y、Z、W四种短周期元素在周期表中的相对位置如右图所示,其中X与W的质子数之和为21,由此可知( )
| |
X |
|
Y |
| Z |
|
W |
|
A.X位于元素周期表中第2周期、第VA族
B.Y的氢化物(H2Y)不稳定,100℃以上即可分解
C.Z的最高价氧化物的水化物是一种强碱
D.W的非金属性比Y的非金属性弱
下列电离方程式书写正确的是()
A.H2S 2H++S2- 2H++S2- |
B.Al(OH)3==Al3+ + 3OH- |
C.NH3·H2O NH4+ +OH- NH4+ +OH- |
D.NaHCO3 ==Na++ H+ + CO32- |
下列物质属于强电解质且该状态下能导电的是:()
(1)氯化钠溶液;(2)氯化铵固体;(3)铜;(4)石墨;
(5)熔融NaOH;(6)稀硫酸;(7)乙酸;
| A.(1)(2)(5)(6) | B.(5) |
| C.(2)(5) | D.(1)(3)(4)(5)(6) |
从下列事实,不能用勒夏特列原理解释的是( )
A.在溴水中存在如下平衡:Br2+H2O  HBr+HBrO当加入NaOH溶液后颜色变浅 HBr+HBrO当加入NaOH溶液后颜色变浅 |
B.对   平衡体系增加压强使颜色变深 平衡体系增加压强使颜色变深 |
C.反应  CO2+NO△H<0升高温度使平衡向逆方向移动 CO2+NO△H<0升高温度使平衡向逆方向移动 |
D.合成氨反应: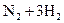   ,△H<0 为使氨的产率提高,理论上应采取低温高压的措施 ,△H<0 为使氨的产率提高,理论上应采取低温高压的措施 |
密闭容器中,反应2X(g) Y(g)+Z(s)已达到平衡,下列叙述正确的是()
Y(g)+Z(s)已达到平衡,下列叙述正确的是()
| A.若升高温度,X(g)的浓度增大,则正反应为吸热反应 |
| B.若容器体积不变,在平衡混合物中加入少量Z(s),则平衡向左移动 |
| C.压强变化对该平衡没有影响 |
| D.若容器体积不变,加入氦气平衡不移动 |
14CO2与碳在高温条件下发生反应:14CO2+C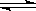 2CO,达到化学平衡后,平衡混合物中含14C的微粒有()
2CO,达到化学平衡后,平衡混合物中含14C的微粒有()
| A.14CO2 | B.14CO2、14CO | C.14CO2、14CO、14C | D.14CO |