一定条件下,在体积为1 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g) Z(g),下列叙述能证明该反应已达到化学平衡状态的是
Z(g),下列叙述能证明该反应已达到化学平衡状态的是
| A.X的百分含量不再发生变化 |
| B.c(X):c(Y):c(Z) =2:1:1 |
| C.容器内气体的质量不再发生变化 |
| D.同一时间内消耗2n mol X的同时生成n mol Z |
下列反应的离子方程式正确的是( )
| A.碳酸钙跟醋酸反应:CaCO3+2H+===Ca2++H2O+CO2↑ |
| B.硫酸铝溶液中加过量氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH4+ |
| C.向足量的溴化亚铁溶液中通入少量氯气:2Fe2++4Br-+3Cl2==2Fe3++2Br2+6Cl- |
| D.碳酸氢钠溶液与足量的氢氧化钡溶液混合: |
Ba2++2OH-+2HCO3—===BaCO3↓+CO32—+2H2O
化学中常用图像直观地描述化学反应的进程或结果。下列对图像描述正确的是( )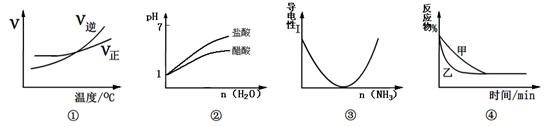
A.根据图①可判断可逆反应A2(g)+3B2(g)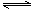 2AB3(g)的ΔH>0 2AB3(g)的ΔH>0 |
| B.图②表示体积相等、pH=1的醋酸溶液与盐酸加入等量水稀释时的pH变化 |
| C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
D.图④可表示压强对可逆反应2A(g)+2B(g)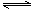 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
不能鉴别AgNO3、BaCl2、Na2CO3、MgCl2四种溶液(不考虑它们之间的相互反应)的试剂是( )
| A.盐酸、硫酸 | B.盐酸、NaOH溶液 | C.氨水、硫酸 | D.氨水、NaOH溶液 |
可逆反应2A(g)+aB(?) 2C(g)+D(g),其中a为正整数。反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是( )
2C(g)+D(g),其中a为正整数。反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是( ) 
| A.达到平衡后,加入催化剂则C%增大 |
| B.达到平衡后,若升高温度,平衡向右移动 |
| C.a可以为任意的正整数 |
| D.达平衡后,增加B的量,有利于平衡向右移动 |
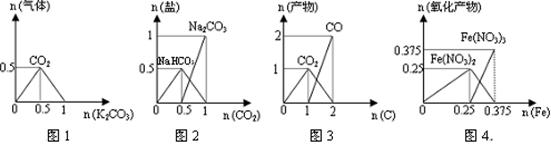
下列图象能正确表示相关反应中产物物质的量的变化的是(横、纵坐标单位:mol)
| A.图1:n(HCl)=1mol,K2CO3逐步加入到HCl溶液中,在敞口容器中生成的气体 |
| B.图2:n(NaOH)=1mol,CO2逐步通入到NaOH溶液中反应生成的盐 |
| C.图3:n(O2)=1mol,高温下C和O2在密闭容器中的反应产物 |
| D.图4:n(HNO3)=1mol,Fe和稀HNO3反应生成的氧化产物(还原产物为NO) |