下列操作达不到预期目的的是( )
①将某卤代烃与氢氧化钠的水溶液共热,向冷却后的反应液中滴加AgNO3溶液,若产生白色沉淀,则证明该卤代烃为氯代烃
②用乙醇和30%的硫酸共热到170℃制取乙烯
③在苯酚稀溶液中逐滴滴入饱和溴水出现白色沉淀
④将苯与浓硝酸混合加热至60℃制备硝基苯
| A.①③④ | B.②③ | C.①②④ | D.①②③④ |
已知33As、35Br位于同一周期,下列关系正确的是
A 原子半径:As>C1>P B 热稳定性:HC1>AsH3>HBr
C 还原性:As3->S2->C1-D 酸性:H3AsO4>H2SO4>H3PO4
是部分短周期元素化合价与原子序数的关系图,下列说法正确的是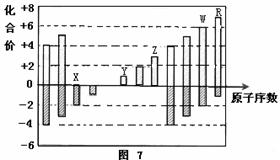
| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性:R>W |
| C.WX和水反应形成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物相互不能反应 |
被称为万能还原剂的NaBH4溶于水并和水反应:NaBH4+2H2O=NaBO2+4H2↑,下列说法中正确的是(NaBH4中H为-1价)
| A.NaBH4既是氧化剂又是还原剂 |
| B.NaBH4是氧化剂,H2O是还原剂 |
| C.硼元素被氧化,氢元素被还原 |
| D.被氧化的元素与被还原的元素质量之比为1∶1 |
ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室中可通过以下反应制得:2KClO3+H2C2O4+H2SO4 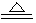 2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是
2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是
| A.CO2是氧化产物 |
| B.H2C2O4在反应中被氧化 |
| C.H2C2O4的氧化性强于ClO2的氧化性 |
| D.ClO2作水处理剂时,利用了其强氧化性 |
用高铁酸钠(Na2FeO4)对水消毒是城市饮用水处理的新技术。已知反应:Fe2O3+3Na2O2=2Na2FeO4+Na2O,下列说法正确的是
| A.Na2O2既是氧化剂又是还原剂 |
| B.Na2FeO4既是氧化产物又是还原产物 |
| C.3 mol Na2O2发生反应,有12 mol电子转移 |
| D.在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌 |