在一个不传热且容积固定的密闭反应器里,有可逆反应:mA(g) + nB(g) 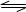 pC(g)+qD(g) 当m、n、p、q为任意正整数时,该反应达到平衡的标志是( )
pC(g)+qD(g) 当m、n、p、q为任意正整数时,该反应达到平衡的标志是( )
①体系的压强不再发生变化;
②体系的温度不再发生变化;
③各组分的物质的量浓度不再发生变化;
④各组分的质量分数不再发生变化;
⑤反应速率γA:γB: γC: γD = m:n:p:q;
⑥单位时间内,若消耗了m mol A物质,同时也消耗了qmolD物质
| A.①③⑤ | B.①④⑥ | C.②③④⑥ | D.③④⑤⑥ |
已知H—H键能436 kJ/mol;Cl—Cl键能243kJ/mol;H—Cl键能431 kJ/mol,则下列热化学方程式正确的是
| A.H2(g)+Cl2(g)="2HCl(g)" ΔH=-183 kJ/mol |
| B.1/2H2(g)+1/2Cl2(g)="HCl(g)" ΔH=-124kJ/mol |
| C.2HCl(g)=H2(g)+Cl2(g) ΔH=-248 kJ/mol |
| D.HCl(g) =1/2H2(g)+1/2Cl2(g) ΔH=-91.5 kJ/mol |
下图中a、b是惰性电极,通电2 min后b电极附近溶液呈红色,b电极生成标准状况时的气体体积为2.24L,NaCl溶液体积为500 mL,下列说法不正确的是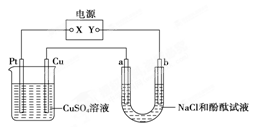
| A.电解过程中CuSO4溶液物质的量浓度不变 |
| B.电子流动的方向是由a流向Cu电极 |
| C.电路中通过的电子为0.2mol, |
| D.电解速率v(OH-)=0.2mol/(L.min) |
已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是285.8kJ·mol-1、1411.0kJ·mol-1和1366.8 kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为
| A.-44.2 kJ·mol-1 | B.+44.2 kJ·mol-1 | C.-330 kJ·mol-1 | D.+330 kJ·mol-1 |
25℃时,将pH=3的HA溶液与pH=11的BOH溶液等体积混合,所得溶液pH小于7。下列说法不正确的是
| A.HA为弱酸 |
| B.混合溶液中加水稀释,pH升高,溶液导电能力减弱 |
| C.等物质的量浓度等体积的NaA与NaCl溶液,溶液中的离子数目相等 |
| D.混合溶液中滴加氨水至溶液的pH=7,所得溶液中c(A-)=c(NH)+c(B+) |
常温下,有下列四种溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液。下列有关说法正确的是
| A.①、②、④溶液分别与足量铝粉反应,生成H2的量:②最少 |
| B.四种溶液的KW相同,由水电离的c(H+):①=③>②=④ |
| C.将①、④两种溶液混合后,若pH=7,消耗溶液的体积为:①>④ |
| D.向等体积的四种溶液中分别加入1000 mL水后,溶液的pH:③>④>②>① |