设NA为阿伏加德罗常数, 下列说法正确的是
| A.1.8g 水所含有的电子数目为NA |
| B.2g 氢气所含原子数为NA |
| C.常温常压下11.2L氧气所含分子数目为0.5NA |
| D.200 mL0.5mol·L-1 Na2SO4溶液所含Na+数目0.1NA |
如下图所示的装置能够组成原电池且产生电流的是( )
下列烧杯中盛放的都是稀硫酸,在铜电极上能产生气泡的是( )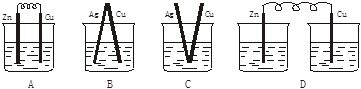
已知3.6 g碳在6.4 g的氧气中燃烧,至反应物耗尽,并放出X kJ热量。已知单质碳的燃烧热为-Y kJ/mol,则C与1mol O2反应生成CO时的反应热ΔH为()
| A.-Y kJ/mol | B.-(10X-Y) kJ/mol |
| C.-(5X-0.5Y) kJ/mol | D.+(10X-Y) kJ/mol |
航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,点燃时铝粉氧化引发高氯酸铵反应,其方程式可表示为: NH4ClO4=N2↑+4H2O+Cl2↑+2O2↑;△H<0 下列对此反应的叙述中错误的是()
| A.上述反应属于分解反应 |
| B.上述反应瞬间产生大量高温气体推动航天飞机飞行 |
| C.反应从能量变化上说,主要是化学能转变为热能和动能 |
| D.在反应中高氯酸铵只能起氧化剂作用 |
在一定条件下,CO和CH4燃烧的热化学方程式分别为:
2CO(g) + O2(g) = 2CO2(g);ΔH ="-566" kJ/mol
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l); ΔH ="-890" kJ/mol
由1molCO和3molCH4组成的混和气在上述条件下完全燃烧时,释放的热量为()
| A.2912kJ | B.2953kJ | C.3236kJ | D.3867kJ |