下列有关化学用语使用正确的是
A.硫原子的原子结构示意图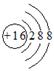 |
| B.乙烯的结构简式CH2CH2 |
| C.NaHSO4在熔融状态下的电离方程式:NaHSO4=Na++H++SO42- |
D.质子数为53,中子数为78的碘原子: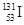 |
德国重离子研究中心于2010年2月19日宣布,以国际纯粹与应用化学联合会确认,由该中心合成的第112号化学元素从即日起获正式名称“Copernicium”,相应的元素符号为“Cn”。选择2月19日为新元素正式冠名日,也是因为这一天是哥白尼的生日,有报道称Cn原子含有165个中子。下列有关112号元素的相关说法正确的是
A.该原子可表示为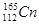 |
| B.该元素应位于元素周期表的第7周期ⅡB族 |
| C.该元素的相对原子质量为277 |
| D.该原子能够稳定存在 |
化学与生活、社会密切相关。下列说法正确的是
| A.红宝石、珍珠、玛瑙、水晶、钻石等装饰品的主要成分都是硅酸盐 |
| B.氢氧燃料电池、铅蓄电池、硅太阳能电池中都利用了原电池原理 |
| C.NO可用于某些疾病的治疗;SO2可用于食品防腐剂 |
| D.明矾可用于水的消毒、杀菌;硫酸钡可用于钡餐透视 |
右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是
| A.该试剂的物质的量浓度为9.2 mol/L |
| B.该硫酸50 mL若用5 mol/L的氢氧化钠中和,需要该氢氧化钠溶液100毫升 |
C.该硫酸与等体积的水混合所得溶液的质量分 数等于49% 数等于49% |
| D.配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL |
将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度为
A. mol/L mol/L |
B. mol/L mol/L |
C.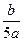 mol/L mol/L |
D. mol/L mol/L |