对于某温度下平衡体系mA(g) + nB(g) pC(g) + qD(g) △H<0,下列说法不正确的是:
pC(g) + qD(g) △H<0,下列说法不正确的是:
A.若温度不变将容器容积扩大到原来的2倍,此时A的浓度变为原来的0.52倍,则m + n > p + q
B.向平衡体系中加入C、D,该反应的△H减小
C.若温度和容器体积不变,充入一定量的惰性气体,B的浓度不变
D.若平衡时,增加A的量,A的转化率下降,B的转化率增加
下列事实不能用勒夏特列原理解释的是
| A.打开汽水瓶有气泡从溶液中冒出 |
| B.实验室用排饱和食盐水法收集氯气 |
| C.合成氨工厂采用增大压强以提高原料的转化率 |
D.2NO2(g)  N2O4(g)的平衡体系中,加压缩小体积后颜色加深 N2O4(g)的平衡体系中,加压缩小体积后颜色加深 |
在下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是
| A.2Na2O2+2H2O=4NaOH+O2↑ |
| B.Mg2N2+6H2O=3Mg(OH)2↓+2NH3↑ |
| C.Cl2+H2O=HClO+HCl |
D.NH4Cl+NaOH NaCl+NH3↑+H2O NaCl+NH3↑+H2O |
在一定温度下,恒容密闭容器中,充入一定量的NO和O2,发生反应O2(g)+2NO(g)  2NO2(g),反应已达到平衡的标志是
2NO2(g),反应已达到平衡的标志是
| A.反应混合物中各组分的浓度相等 |
| B.混合气体的密度不再改变 |
| C.混合气体的颜色不再变化 |
| D.O2、NO、NO2三种物质的反应速度之比为1﹕2﹕2 |
下列分子或离子中,含有孤对电子的是
| A.H2O | B.CH4 | C.SiH4 | D.NH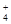 |
常温下,下列各组离子能够大量共存的是
| A.pH=0的溶液中:Fe3+、Mg2+、Cl-、SO42- |
| B.使pH试纸显蓝色的溶液中:Cu2+、Fe3+、NO3-、SO32- |
| C.滴入甲基橙指示剂呈红色的溶液中:Na+、NH4+、CO32-、NO3- |
| D.水电离出的c(H+)=1×10-13mol·L-1的溶液中:K+、HCO3-、Cl-、NH4+ |