下列物质在水溶液中的电离方程式书写正确的是( )
| A.CaCl2=Ca2++2Cl- | B.K2CO3=K2++CO32- |
| C.Ba(OH)2=Ba 2++(OH)2- | D.FeCl3=Fe2++3Cl- |
下列各组离子反应可用H++OH-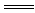 H2O表示的是()
H2O表示的是()
| A.氢氧化钡和硫酸 | B.氢氧化铁和盐酸 |
| C.硝酸和氢氧化钠 | D.碳酸氢钠和氢氧化钠 |
下列关于钠的叙述中,不正确的是()
| A.钠燃烧时发出黄色的火焰,生成过氧化钠 |
| B.钠应保存在煤油中 |
| C.钠有很强的还原性 |
| D.金属钠着火时,可以用水灭火 |
下列物质中,能够导电的电解质是()
| A.Cu丝 | B.熔融的MgCl2 | C.NaCl溶液 | D.蔗糖 |
下列电离方程式错误的是()
A.Ba(OH)2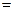 Ba2+ +2OH- Ba2+ +2OH- |
B.NaHSO4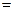 Na+ +H+ +SO42- Na+ +H+ +SO42- |
C.MgC l2 l2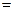 Mg2+ +2Cl- Mg2+ +2Cl- |
D.NaHCO3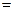 Na+ +H+ +CO32- Na+ +H+ +CO32- |
下列说法正确的是()
| A.可用丁达尔现象区分溶液与胶体 |
| B.生石灰与水混合的过程只发生物理变化 |
| C.胶体是一种纯净物 |
| D.CuSO4·5H2O是一种混合物 |