下列对有关实验的描述不正确的是( )
| A.在浓氨水中加入生石灰可以制取少量的NH3 |
B.用惰性电极电解熔融NaCl:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| C.氯水和活性炭使红墨水褪色,能用同一原理解释 |
| D.浓硫酸和浓盐酸长期暴露在空气中浓度都会降低 |
下列离子方程式书写正确的是
| A.向NaHSO4溶液中滴入Ba(OH)2溶液至中性:H++SO42-+Ba2++OH- = BaSO4↓+H2O |
| B.NaClO溶液与FeCl2溶液混合:Fe2+ + 2ClO- + 2H2O = Fe(OH)2↓ + 2HClO |
| C.NH4HSO3溶液与足量NaOH溶液反应:NH4+ + OH-= NH3↑ + H2O |
| D.将1mol/LNaAlO2溶液和1.5mol/L的HCl溶液等体积均匀混合:6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+ |
酚酞医药名为果桃,可治疗消化系统疾病,其有效成分的结构简式如图所示。下列对该有效成分的说法正确的是()
| A.所有原子可能共平面 |
| B.能发生加聚反应生成高分子化合物 |
| C.酚酞的水解产物中含有醇羟基 |
| D.1 mol该物质最多能与含4 mol NaOH的烧碱溶液反应 |
已知:乙醇可被强氧化剂氧化为乙酸。 可经三步反应制取
可经三步反应制取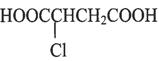 ,其中第二步的反应类型是
,其中第二步的反应类型是
| A.加成反应 | B.水解反应 | C.氧化反应 | D.消去反应 |
从下列事实所得出的结论或给出的解释正确的是
| 实验事实 |
结论或解释 |
|
| A |
将40 g NaOH溶于1 L蒸馏水中 |
该溶液的物质的量浓度为1mol﹒L-1 |
| B |
0.1 mol/L CH3COOH溶液在稀释过程中 |
 将变小 将变小 |
| C |
酸H2X为弱酸 |
常温下,盐NaHX溶液pH一定大于7 |
| D |
在溶液的稀释过程中 |
离子浓度:有的可能增大,有的可能减小,有的可能不变 |
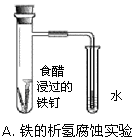
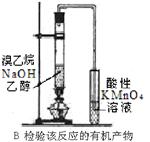
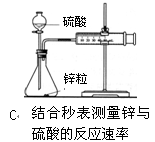
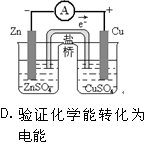
下列装置或操作不能达到实验目的的是()