在1 L HNO3和H2SO4的混合溶液中,两种酸的物质的量浓度之和为0.6 mol/l,向该溶液中加入足量铜粉,加热,充分反应,当HNO3与H2SO4的物质的量比为x:y 时所得溶液中Cu2+物质的量浓度最大,则x:y为
| A.2:3 | B.3:8 | C.1:4 | D.1:1 |
已知C(s)+H2O(g) CO(g)+H2(g) ΔH=AkJ·mol-1
CO(g)+H2(g) ΔH=AkJ·mol-1
2C(s)+O2(g) 2CO(g)ΔH="-220" kJ·mol-1
2CO(g)ΔH="-220" kJ·mol-1
H—H、O O和O—H键的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,则A为
O和O—H键的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,则A为
| A.-332 | B.-118 | C.+350 | D.+130 |
下列有关物质浓度关系的描述,正确的是
| A.25℃时,NaB溶液的pH=8,C(Na+)-C(B-)=9.9×10-7mol/L |
| B.常温下,将醋酸钠和盐酸两溶液混合后溶液呈中性,则混合后的溶液中C(Na+)>C(Cl-)>C(CH3COOH) |
| C.向含有硫酸钡沉淀的溶液中加入Na2SO4固体,C(Ba2+)不变 |
| D.相同条件下,浓度均为0.1 mol/L的NH4Cl溶液和NaCl溶液中,前者的阳离子总浓度大于后者的阳离子总浓度 |
下列有关电解质溶液的说法正确的是
| A.在蒸馏水中滴加浓H2SO4,Kw不变 |
| B.CaCO3难溶于稀硫酸,也难溶于醋酸 |
| C.在Na2S稀溶液中,C(H+)=C(OH-)-2C(H2S) -C(HS-) |
| D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
科研人员设想用如图所示装置生产硫酸,下列说法正确的是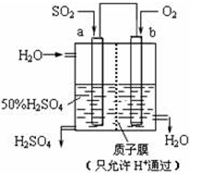
| A.A为正极,B为负极 |
| B.生产过程中A电极质量减轻 |
| C.电子从B极向A极移动 |
| D.负极反应式为:SO2-2e-+ 2H2O = SO42-+ 4H+ |
如图所示,A、B是多孔石墨电极,某同学按图装置进行如下实验:断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转。下列说法不正确的是
A.断开K2,闭合K1时,A极上的电极反应式为:4OH¯一4e¯===O2↑十+2H2O
B.断开K2,闭合K1一段时间,溶液的pH要变大
C.断开K1,闭合K2时,B极上的电极反应式为: 2H++2e¯===H2↑
D.断开K1,闭合K2时,OH¯向B极移动