将3.22克Na2SO4 ·10H2O 溶于水中,要使Na+离子数目与水分子数目之比为1:100,则加入水的质量为
| A.18 | B.36 | C.34.2 | D.37.8 |
下图是某同学用500 mL容量瓶配制0.10 mol·L-1 NaOH溶液的过程:
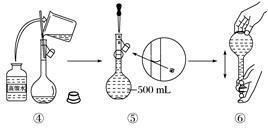
该同学的错误步骤有
| A.1处 | B.2处 | C.3处 | D.4处 |
下列有关物质性质的应用正确的是
| A.石英坩埚耐高温,可用来加热熔化NaOH固体 |
| B.浓硫酸有脱水性,可用作干燥剂 |
| C.二氧化硫有漂白性,可大量用于加工漂白食品 |
| D.医用酒精能使蛋白质变性,可用来消毒杀菌 |
下列有关化学用语表示正确的是
A.过氧化钠的电子式: |
B.质子数为35、中子数为45的溴原子: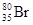 |
C.硫离子的结构示意图: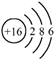 |
D.间二甲苯的结构简式: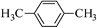 |
下列物质的分类正确的是
| 碱 |
酸 |
盐 |
碱性氧化物 |
酸性氧化物 |
|
| A |
Na2CO3 |
H2SO4 |
NaOH |
SO2 |
CO2 |
| B |
NaOH |
HCl |
NaCl |
Na2O |
NO |
| C |
KOH |
HNO3 |
CaCO3 |
CaO |
Mn2O7 |
| D |
NaOH |
HCl |
CaF2 |
Na2O2 |
SO2 |
N2的结构可以表示为 ,CO的结构可以表示为
,CO的结构可以表示为 ,其中椭圆框表示π键,下列说法中不正确的是
,其中椭圆框表示π键,下列说法中不正确的是
| A.N2分子与CO分子中都含有叁键 | B.CO分子中有一个π键是配位键 |
| C.N2与CO互为等电子体 | D.N2与CO的化学性质相同 |