下列判断中,正确的是
| A.已知25 ℃时NH4CN显碱性,则25 ℃时的电离常数K(NH3·H2O)>K(HCN) |
| B.25 ℃时,Mg(OH)2固体在20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1 NH4Cl溶液中的Ksp小 |
| C.pH试纸测得新制氯水的pH为4 |
| D.FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3 |
用下图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是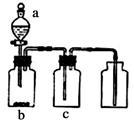
| 气体 |
a |
b |
c |
|
| A |
NH3 |
浓氨水 |
生石灰 |
浓硫酸 |
| B |
NO2 |
浓硝酸 |
铜片 |
NaOH溶液 |
| C |
SO2 |
浓硫酸 |
铜片 |
酸性KMnO4溶液 |
| D |
CO2 |
稀硫酸 |
Na2CO3固体 |
浓硫酸 |
膳食纤维具有突出的保健功能,是人体的“第七营养素”。木质素是一种非糖类膳食纤维,其单体之一—芥子醇结构简式如下图所示。下列有关芥子醇的说法正确的是
| A.芥子醇分子中有五种官能团 |
| B.芥子醇分子中所有碳原子不可能在同一平面上 |
| C.芥子醇与足量浓溴水反应,最多消耗3 mol Br2 |
| D.芥子醇能发生的反应类型有氧化、取代、加成 |
下列解释实验现象的反应方程式正确的是
| A.切开的金属Na暴露在空气中,光亮表面逐渐变暗2Na+O2 = Na2O2 |
| B.向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色2AgCl+S2-=Ag2S↓+2Cl- |
| C.Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物2Na2O2+2CO2=2Na2CO3+O2 |
| D.向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
可逆反应:2NO2(g)  2NO(g)+ O2(g) 在体积不变的密闭容器中进行,达到平衡状态的标志是
2NO(g)+ O2(g) 在体积不变的密闭容器中进行,达到平衡状态的标志是
①单位时间内消耗n mol O2的同时消耗2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
| A.①③④ | B.②③⑤ | C.①④ | D.①②③④⑤ |
如图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是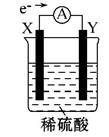
| A.外电路的电流方向为X→外电路→Y |
| B.若两电极分别为铁和碳棒,则X为碳棒,Y为铁 |
| C.X极上发生的是还原反应,Y极上发生的是氧化反应 |
| D.若两电极都是金属,则它们的活动性顺序为X>Y |